题目内容
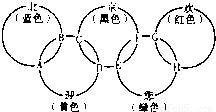
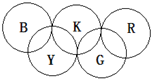 如图所示,形成奥运五环的B、K、R、Y和G均为元素周期表前20号元素的代号,它们还满足下列关系:
如图所示,形成奥运五环的B、K、R、Y和G均为元素周期表前20号元素的代号,它们还满足下列关系:①相邻或相交的两元素均能形成常见化合物.
②B是周期表中原子半径最小的元素.
③K是地壳含量最多的元素,且Y、K两元素同主族.
④G是组成有机化合物的必备元素.
⑤R与其它四种元素既不在同周期,也不在同族.回答下列问题:
(1)K元素在元素周期表中的位置是第
二
二
周期第ⅥA
ⅥA
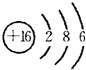
族.(2)Y的原子结构示意图为



(3)B与K形成的化合物与R和G形成的化合物发生反应可用于实验室制取某常见气体,写出该反应的化学方程式
CaC2+2H2O=Ca(OH)2+C2H2↑
CaC2+2H2O=Ca(OH)2+C2H2↑
.(4)任写一个能证明Y和K的非金属性强弱的反应方程式为
2H2S+O2=2S+2H2O
2H2S+O2=2S+2H2O
.分析:如图所示,形成奥运五环的B、K、R、Y和G均为元素周期表前20号元素的代号,它们还满足下列关系:
②B是周期表中原子半径最小的元素,则B为氢元素;③K是地壳含量最多的元素,则K为氧元素;Y、K两元素同主族,则Y为硫元素;④G是组成有机化合物的必备元素,则G为碳元素.⑤R与其它四种元素既不在同周期,也不在同族,则R处于第四周期,故R为钙元素.
②B是周期表中原子半径最小的元素,则B为氢元素;③K是地壳含量最多的元素,则K为氧元素;Y、K两元素同主族,则Y为硫元素;④G是组成有机化合物的必备元素,则G为碳元素.⑤R与其它四种元素既不在同周期,也不在同族,则R处于第四周期,故R为钙元素.
解答:解:如图所示,形成奥运五环的B、K、R、Y和G均为元素周期表前20号元素的代号,它们还满足下列关系:
②B是周期表中原子半径最小的元素,则B为氢元素;③K是地壳含量最多的元素,则K为氧元素;Y、K两元素同主族,则Y为硫元素;④G是组成有机化合物的必备元素,则G为碳元素.⑤R与其它四种元素既不在同周期,也不在同族,则R处于第四周期,故R为钙元素.
故B为氢元素;K为氧元素;Y为硫元素,G为碳元素,R为钙元素.
(1)由上述分析可知,K为氧元素,元素原子有2个电子层,最外层电子数为6,处于周期表第二周期第ⅥA族.
故答案为:二、ⅥA.
(2)Y为硫元素,质子数为16,原子核外有16个电子,有3个电子层,最外层电子数为6,原子结构化示意图为 ;B为氢元素,K为氧元素,R为钙元素.三元素形成的化合物为Ca(OH)2,氢氧化钙属于离子化合物,由钙离子与氢氧根离子构成,电子式为
;B为氢元素,K为氧元素,R为钙元素.三元素形成的化合物为Ca(OH)2,氢氧化钙属于离子化合物,由钙离子与氢氧根离子构成,电子式为 .
.
故答案为: ;
; .
.
(3)B为氢元素;K为氧元素;G为碳元素,R为钙元素.B与K形成的化合物与R和G形成的化合物发生反应可用于实验室制取某常见气体,为碳化钙与水反应生成氢氧化钙与乙炔,制备乙炔,该反应的化学方程式为
CaC2+2H2O=Ca(OH)2+C2H2↑.
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑.
(4)K为氧元素,Y为硫元素.利用单质的氧化性强于氧化产物的氧化性,可以证明元素的非金属性,反应2H2S+O2=2S+2H2O,可说明非金属性O强于S.
故答案为:2H2S+O2=2S+2H2O.
②B是周期表中原子半径最小的元素,则B为氢元素;③K是地壳含量最多的元素,则K为氧元素;Y、K两元素同主族,则Y为硫元素;④G是组成有机化合物的必备元素,则G为碳元素.⑤R与其它四种元素既不在同周期,也不在同族,则R处于第四周期,故R为钙元素.
故B为氢元素;K为氧元素;Y为硫元素,G为碳元素,R为钙元素.
(1)由上述分析可知,K为氧元素,元素原子有2个电子层,最外层电子数为6,处于周期表第二周期第ⅥA族.
故答案为:二、ⅥA.
(2)Y为硫元素,质子数为16,原子核外有16个电子,有3个电子层,最外层电子数为6,原子结构化示意图为
 ;B为氢元素,K为氧元素,R为钙元素.三元素形成的化合物为Ca(OH)2,氢氧化钙属于离子化合物,由钙离子与氢氧根离子构成,电子式为
;B为氢元素,K为氧元素,R为钙元素.三元素形成的化合物为Ca(OH)2,氢氧化钙属于离子化合物,由钙离子与氢氧根离子构成,电子式为 .
.故答案为:
 ;
; .
.(3)B为氢元素;K为氧元素;G为碳元素,R为钙元素.B与K形成的化合物与R和G形成的化合物发生反应可用于实验室制取某常见气体,为碳化钙与水反应生成氢氧化钙与乙炔,制备乙炔,该反应的化学方程式为
CaC2+2H2O=Ca(OH)2+C2H2↑.
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑.
(4)K为氧元素,Y为硫元素.利用单质的氧化性强于氧化产物的氧化性,可以证明元素的非金属性,反应2H2S+O2=2S+2H2O,可说明非金属性O强于S.
故答案为:2H2S+O2=2S+2H2O.
点评:考查结构性质与位置关系、常用化学用语、元素周期律等,难度不大,注意基础知识的掌握与理解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
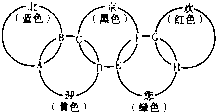 “北、京、欢、迎、您”分别代表五种不同颜色的单质,它们之间相互交叉形成了如图所示的奥运五环旗,A、B、C、D、E、F、G、H是由相交叉的两环元素组成的化合物.
“北、京、欢、迎、您”分别代表五种不同颜色的单质,它们之间相互交叉形成了如图所示的奥运五环旗,A、B、C、D、E、F、G、H是由相交叉的两环元素组成的化合物. 北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣.璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应.请回答下列问题:
北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣.璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应.请回答下列问题: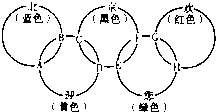 “北、京、欢、迎、您”分别代表五种不同颜色的单质,它们之间相互交叉形成了如图所示的奥运五环旗,A、B、C、D、E、F、G、H是由相交叉的两环元素组成的化合物.
“北、京、欢、迎、您”分别代表五种不同颜色的单质,它们之间相互交叉形成了如图所示的奥运五环旗,A、B、C、D、E、F、G、H是由相交叉的两环元素组成的化合物.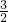 Cl2(g)=PCl3(g);△H=-287.7kJ/mol,P(s)+
Cl2(g)=PCl3(g);△H=-287.7kJ/mol,P(s)+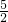 Cl2(g)=PCl5(g);△H=-498.7kJ/mol.则PCl5(g)分解生成PCl3(g)和Cl2(g)反应的热化学方程式为:______.
Cl2(g)=PCl5(g);△H=-498.7kJ/mol.则PCl5(g)分解生成PCl3(g)和Cl2(g)反应的热化学方程式为:______.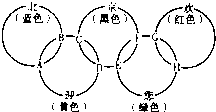
 Cl2(g)=PCl3(g);△H=-287.7kJ/mol,P(s)+
Cl2(g)=PCl3(g);△H=-287.7kJ/mol,P(s)+ Cl2(g)=PCl5(g);△H=-498.7kJ/mol.则PCl5(g)分解生成PCl3(g)和Cl2(g)反应的热化学方程式为:______.
Cl2(g)=PCl5(g);△H=-498.7kJ/mol.则PCl5(g)分解生成PCl3(g)和Cl2(g)反应的热化学方程式为:______.