题目内容
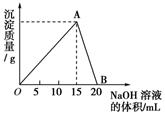
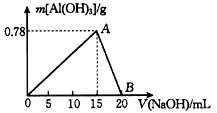
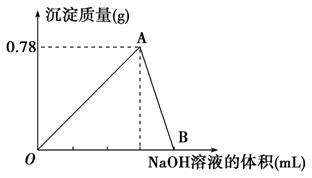
向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol·L-1 NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加NaOH溶液的体积( mL)关系如下图所示,试回答下列问题:
(1)图中A点表示的意义是____________________________。
(2)图中B点表示的意义是____________________________。
(3)上述两步反应用总的离子方程式可表示为____________________________。
(4)假若溶液中有Al(OH)3沉淀
解析:由图可知,随着NaOH溶液的加入,溶液中发生由Al3+→Al(OH)3→![]() 的转化。故A点表示得到Al(OH)3沉淀的最大值,B点表示Al(OH)3沉淀完全溶解,涉及的离子方程式为:
的转化。故A点表示得到Al(OH)3沉淀的最大值,B点表示Al(OH)3沉淀完全溶解,涉及的离子方程式为:
Al3++3OH-![]() Al(OH)3↓,Al(OH)3+OH-
Al(OH)3↓,Al(OH)3+OH-![]()
![]() +2H2O
+2H2O
总的离子方程式为:Al3++4OH-![]()
![]() +2H2O
+2H2O
通过上面图象可知,要生成
答案 (1)生成Al(OH)3沉淀的最大值
(2)Al(OH)3沉淀完全溶解于NaOH溶液成为NaAlO2溶液
(3)Al3++4OH-![]()
![]() +2H2O
+2H2O
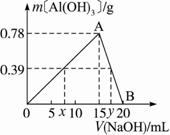
(4)7.5 mL或17.5 mL

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目