题目内容
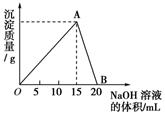
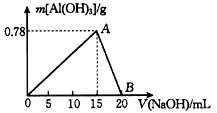
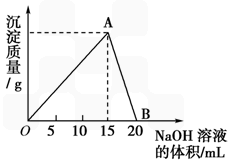
向20 mL某浓度的AlCl3溶液中滴加2 mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如下图所示:
(1)图中A点表示的意义是_____________________________________________。
(2)最大沉淀量为________g。
(3)B点表示的意义是_________________________________________________。
(4)所用AlCl3溶液的物质的量浓度是________。
(5)当所得沉淀量为0.39 g时,用去NaOH溶液的体积是________mL或________mL。
(1)AlCl3与NaOH恰好完全反应,得到最大沉淀量 (2)0.78
(3)Al(OH)3与NaOH恰好完全反应生成NaAlO2,沉淀完全溶解
(4)0.5 mol·L-1 (5)7.5 17.5
解析试题分析:本题是AlCl3与NaOH反应与图象相结合的问题,考查了大家对图象的解读能力,分析问题能力、计算能力等。本题解决的关键是明确NaOH溶液逐滴加入到AlCl3溶液中的反应情况:开始AlCl3与NaOH生成Al(OH)3沉淀,NaOH量逐渐增多,Al(OH)3量逐渐增大,当将AlCl3恰好完全沉淀时,Al(OH)3沉淀达到最大量,随后再加NaOH,沉淀量又逐渐减少直至消失。由于A→B消耗的氢氧化钠为0.01 mol,则n(AlCl3)=0.01 mol,A处生成Al(OH)3 0.78 g,所用AlCl3的物质的量浓度为0.5 mol·L-1。
(5)当NaOH溶液不足时,生成0.39 g Al(OH)3所需NaOH的物质的量为0.015 mol,当NaOH溶液过量时,还剩余0.39 g Al(OH)3共消耗NaOH 0.035 mol,NaOH溶液的体积分别为7.5 mL和17.5 mL。
考点:铝的图像问题
点评:最后一问用图像法,通过相似三角形解更简单。