题目内容
【题目】在2L密闭容器中充有2molSO2和一定量O2发生下列反应2SO2+O2![]() 2SO3,经4min后测得SO2为0.4mol,则O2的反应速率是
2SO3,经4min后测得SO2为0.4mol,则O2的反应速率是
A. 0.1mol/(L·min)B. 0.2mol/(L·min)
C. 0.3mol/(L·min)D. 0.05mol/(L·min)
【答案】A
【解析】
根据化学反应速率的概念可知,进行到4min时,测得n(SO2)=0.4mol,此时反应的速率为V(SO2)=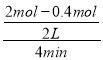 =0.2mol/(L·min),根据用不同物质表示的反应速率时,速率比等于化学方程式的化学计量数的比,所以V(O2)=
=0.2mol/(L·min),根据用不同物质表示的反应速率时,速率比等于化学方程式的化学计量数的比,所以V(O2)=![]() V(SO2)=
V(SO2)=![]() ×0.2mol/(L·min)= 0.1mol/(L·min),所以选项A合理。
×0.2mol/(L·min)= 0.1mol/(L·min),所以选项A合理。

【题目】氯酸钾在工业上具有广泛的应用,是焰火、照明弹等的主要成分。某研究性学习小组利用如图所示的实验装置制备氯酸钾。回答下列问题:
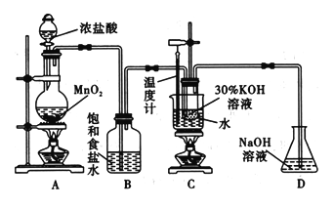
(1)写出装置A中发生反应的离子方程式:________________________________;写出装置C中发生反应的离子方程式:________________________________________。
(2)若无B装置,则装置C中氯酸钾的产率将________(填“提高” “降低”或“无影响”)。
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究体系中硫酸浓度对反应产物的影响,实验的记录表如下表(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0. 20mol L-1KI/mL | V1 | 1.0 | 1.0 | 1.0 |
KC1O3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0mol L-1H2SO4/mL | 0 | 3.0 | V2 | 9.0 |
蒸馏水 | 9.0 | V3 | 3.0 | 0 |
实验现象 |
①实验设计表中V1=____________; V3 =_______________。
②设计1号试管实验的作用是_________________________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色。假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为_____________________________。
(4)工业上可用KC1O3与Na2SO3在H2SO4存在下制备高效、低毒的消毒剂ClO2,该反应的化学方程式为_________________________________。