题目内容
6.指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:Co3+、CN-、6.分析 根据配合物K3[Co(CN)6]结构分析中心离子为Co3+、配体为CN-、配位数为6.
解答 解:根据配合物K3[Co(CN)6]结构分析,含有空轨道的金属阳离子为中心离子,所以中心离子为Co3+、有孤对电子的原子或离子为配体,所以配体为CN-、配位数就是配体的个数,所以配位数为6,
故答案为:Co3+;CN-;6.
点评 本题考查配合物的结构,侧重于配合物组成的分析,题目难度中等.

练习册系列答案
相关题目
16.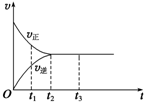 如图是可逆反应X2+3Y2?2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应X2+3Y2?2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
 如图是可逆反应X2+3Y2?2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应X2+3Y2?2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )| A. | t1时,只有正方向反应 | B. | t2时,反应达到限度 | ||
| C. | t2~t3,反应不再发生 | D. | t2~t3,各物质的浓度相等 |
17.与主族元素在元素周期表中所处位置有关的是( )
| A. | 相对原子质量 | B. | 电子层数和最外层电子数 | ||
| C. | 化合价 | D. | 核内中子数 |
14.能够鉴定氯乙烷中存在氯元素的操作是( )
| A. | 在氯乙烷中直接加入AgNO3溶液 | |
| B. | 在氯乙烷中加蒸馏水,然后加入AgNO3溶液 | |
| C. | 在氯乙烷中加入乙醇,加热后酸化,然后加入AgNO3溶液 | |
| D. | 在氯乙烷中加入NaOH溶液,加热后酸化,然后加入AgNO3溶液 |
1.下列说法中错误的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 在共价化合物中一定含有共价键 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 离子化合物中可能含有共价键 |
18.已知中和热的数值是57.3kJ•mol-1.下列物质反应时,产生57.3kJ热量的是( )
| A. | 稀HCl和稀NaOH | |
| B. | 1.0 mol•L-1 HCl和1.0 mol•L-1 NaOH | |
| C. | 500 mL 2.0 mol•L-1 HCl和500 mL2.0 mol•L-1 NaOH | |
| D. | 500 mL 2.0 mol•L-1 H2SO4和500 mL 2.0 mol•L-1 Ba(OH)2 |
15.下列说法正确的是( )
| A. | 用活性炭去除冰箱中的异味是发生了化学反应 | |
| B. | 用热碱水清除炊具上残留的油污,是因为Na2CO3可直接和油污反应 | |
| C. | 用浸泡过高锰酸钾溶液的硅藻土保存水果 | |
| D. | 漂白粉在空气中久置变质是因为漂白粉中的CaCl2 与空气中的CO2反应生成CaCO3 |
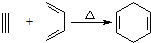 ,请回答下列问题.
,请回答下列问题. ,所用的原料可以是AD
,所用的原料可以是AD .
.