题目内容
【题目】近日,雾霾又上了度娘热搜榜。其主要成分包括灰尘、SO2、NOx、有机碳氢化合物等粒子。烟气脱硝是治理雾霾的方法之一。
(1)氨气是常见的烟气脱硝剂之一,其脱硝原理是与NO(g)反应生成空气中存在的两种无毒物质。
①写出该反应的化学反应方程式:_____________。
②已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H1=-907.28kJ mol-1;
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H2= -1269.02kJ mol-1。105℃时,则上述脱硝反应的△H=_______,该反应________(填“能” “否”或“不能确定”)自发进行,
③上述脱硝反应中氧化剂和还原剂的物质的量之比为________。每生成1mol还原产物,则反应中转移电子数为_________mol。
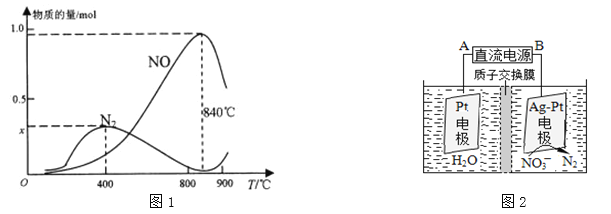
(2)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为2NO2(g)+O3(g)![]() N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生上述反应,相关信息如下表及图所示,回答下列问题:
N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生上述反应,相关信息如下表及图所示,回答下列问题:
容器 | 甲 | 乙 |
容积/L | 1 | 1 |
温度/K | T1 | T2 |
起始充入量 | lmolO3 2mol NO2 | lmolO3 2mol NO2 |
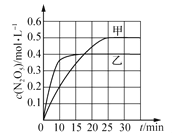
0~10min内甲容器中反应的平均速率:v(O3) =_______mol·L-1·min-1 。
②T1________T2 (填“>”“<”或“=”),T1时,该反应的平衡常数为____________。
③下列措施能提高容器乙中NO2转化率的是________(填序号)。
A.向容器中充入He,增大容器的压强
B.升高容器的温度
C.向容器中再充人一定量的NO2
D.向容器中再充入lmol O3和2mo NO2
④T1时,若起始时向容器甲中充入2mo1 NO2、lmolO3、2mollN2O5和2molO2,则脱硝反应达到平衡前,v(正)________v(逆) (填“>”“<”“=”)。
【答案】4NH3+6NO=5N2+6H2O-1811.63kJ·mol-1能3∶240.02<0.5L·mol-1D<
【解析】
(1)①根据题意,两种无毒物质是水和N2,故反应方程式为4NH3+6NO=5N2_+6H2O;
②已知:①4NH3(g)+5O2(g)=4NO(g)+6H2O(g)____△H1=-907.28kJ__mol-1;②4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H2=_-1269.02kJ__mol-1;根据盖斯定律可知由②×![]() -①×
-①×![]() 得反应4NH3+6NO=5N2_+6H2O,该反应的ΔH=(_-1269.02kJ__mol-1)×
得反应4NH3+6NO=5N2_+6H2O,该反应的ΔH=(_-1269.02kJ__mol-1)×![]() -(-907.28kJ__mol-1)×
-(-907.28kJ__mol-1)×![]() =-1811.63kJ·mol-1;该反应放热,且S_>0,G<0,故反应能自发。
=-1811.63kJ·mol-1;该反应放热,且S_>0,G<0,故反应能自发。
③该反应中氧化剂为NO,还原剂为NH3,物质的量之比为3∶2,且根据氧化剂为NO可知,每生成1mol还原产物,则反应中转移电子数为4mol。
(2)①读图可知,0~10min内甲容器中N2O5的浓度变化量为0.2mol·L-1,2NO2(g)+O3(g)===N2O5(g)+O2(g),则消耗O3的浓度为0.2mol·L-1,反应速率V(O3)=0.02mol·(L·min)-1。
②由图象知,容器乙先达到平衡,温度高,即T1<T2,
2NO2(g)+O3(g)![]() N2O5(g)+O2(g)
N2O5(g)+O2(g)
起始浓度(mol/L) 2 1 0 0
变化浓度(mol/L) 1 0.5 0.5 0.5
平衡浓度(mol/L) 1 0.5 0.5 0.5
T1时,该反应的平衡常数K=![]() =0.5;
=0.5;
③A项,向容器中充入He,增大容器的压强,但不改变反应速率和平衡。B项,由图象知,该反应提高温度,反应逆向进行。C项,向容器中充入一定量的NO2,NO2的转化率降低。D项,向容器中再充入1mol O3和2mol NO2,相当于加压,平衡正向移动;故答案为D;
④若起始时向容器甲中充入2mol NO2、1mol O3、2mol N2O5和2mol O2,计算浓度商Qc=![]() =1,相当于加入五氧化二氮反应逆向进行,则脱硝反应达到平衡前,v(正)<v(逆)。
=1,相当于加入五氧化二氮反应逆向进行,则脱硝反应达到平衡前,v(正)<v(逆)。

 阅读快车系列答案
阅读快车系列答案【题目】中和滴定的相关问题
Ⅰ.下面a~e是中学化学实验中常见的几种定量仪器:
a.量筒 b.容量瓶 c.滴定管 d.托盘天平 e.温度计
(1)无“0”刻度的是 (填字母)。
(2)下列操作合理的是 (填字母)。
A.用25 mL碱式滴定管量取20.00 mL NaOH溶液
B.用托盘天平准确称量10.20 g碳酸钠固体
C.用100 mL量筒量取3.2 mL浓硫酸
D.用500 mL容量瓶配制1 mol·L-1的氢氧化钠溶液495.5 mL
Ⅱ. 某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是 ___(填编号)。
(2)判断滴定终点的现象是: 。
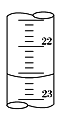
(3)如图是某次滴定时的滴定管中的液面,其读数为 mL。
(4)根据下列数据,请计算待测盐酸的浓度: mol·L-1。
滴定次数 | 待测体积(mL) | 标准烧碱溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 2.00 | 24.10 |
第三次 | 20.00 | 4.00 | 24.00 |
(5)在上述实验中,下列操作(其它操作正确)一定会造成测定结果偏高的是 (填字母)。
A.配制标准溶液的固体NaOH中混有KOH杂质
B.滴定终点读数时,俯视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液