题目内容
下图是一些重要工业生产的转化关系(反应条件略去):
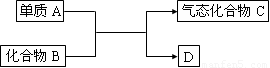
请完成下列问题:
(1)若D是单质,且与A属于同一主族,反应在高温下进行,则:
①此反应的化学方程式是 。
②D单质的一种重要用途是 。
(2)若B为黄色固体,D为固体化合物,则该反应为4FeS2+11O2  2Fe2O3+8SO2
2Fe2O3+8SO2
①当有1molC生成时,该反应转移电子的总数是 。
②将C通入足量的酸性KMnO4 溶液中,发生反应的离子方程式为 。
(3)若B是一种碱性气体,D为化合物,则:
①该反应的化学方程式是 。
②B在加热条件下与CuO反应有Cu生成,该反应的化学方程式为 ;有人提出产物Cu中可能还含有Cu2O。已知Cu+在酸性溶液中不能稳定存在,为验证Cu2O是否存在,可取少量反应产物,滴加足量稀硫酸,若溶液由无色变为蓝色,则证明含有Cu2O。请写出发生反应的化学方程式:_________。
(1)①2C+SiO2
 Si+2CO↑②制半导体材料
Si+2CO↑②制半导体材料
(2)①3.31×1024
②2MnO4-+5SO2+ 2H2O ===2Mn2++5SO42- +4H+
(3)①4NH3+5O2 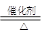 4NO+6H2O
4NO+6H2O
②2NH3+3CuO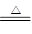 3Cu+N2↑+3H2O Cu2O+H2SO4=Cu+CuSO4+H2O
3Cu+N2↑+3H2O Cu2O+H2SO4=Cu+CuSO4+H2O
【解析】
试题分析:(1)同族之间的高温下单质的置换反应,就只有碳和硅之间的反应。所以①2C+SiO2
 Si+2CO↑②制半导体材料
Si+2CO↑②制半导体材料
(2)此反应中生成8 mol的二氧化硫时,转移44 mol的电子,所以每生成1 mol二氧硫时,转移的电子总数为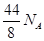 ,也等于3.31×1024
,也等于3.31×1024
②2MnO4-+5SO2+ 2H2O ===2Mn2++5SO42- +4H+
(3)碱性气体只能是氨气。①4NH3+5O2 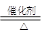 4NO+6H2O
4NO+6H2O
②2NH3+3CuO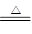 3Cu+N2↑+3H2O Cu2O+H2SO4=Cu+CuSO4+H2
3Cu+N2↑+3H2O Cu2O+H2SO4=Cu+CuSO4+H2
考点:无机物的有关知识。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案