题目内容
(1)理论上需要消耗MnO2多少克?
(2)被氧化的HCl的物质的量是多少?
(2)根据原子守恒计算参加氧化还原反应的盐酸的物质的量.
MnO2+4HCl(浓)
| ||
87g 22.4L
x 1.12L
x=
| 87g×1.12L |
| 22.4L |
答:需要消耗二氧化锰的质量是4.35g;
(2)参加氧化还原反应的盐酸和氯气之间的关系式是2HCl(浓)→Cl2,生成22.4L氯气需要2mol盐酸参加氧化还原反应,则生成1.12L氯气需要0.1mol盐酸参加氧化还原反应,
答:被氧化的HCl的物质的量是0.1mol.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案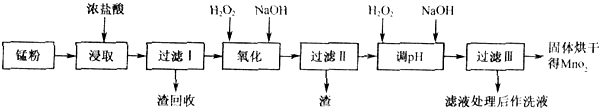
根据如图所示步骤并参考表格数据,回答下列问题.
生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入足量H2O2溶液,其作用是
(3)过滤Ⅰ所得滤液经氧化后,需加入NaOH溶液调节pH约为5.1,其目的是
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为
(5)实验室进行过滤操作时.需要用到的玻璃仪器有
(16分)回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由锰粉制取MnO2的步骤和数据如下:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)2 | 8.3 | 9.8 |
(1)在加热条件下,用浓盐酸浸取锰粉得到含有Mn2+、Fe3+等离子的溶液,MnO2与浓盐酸反应的离子方程式 ,该处理方法的缺点 。
(2)步骤I中滤渣的化学式 ,步骤I中滤渣的化学式 。
(3)向步骤I的滤液中加足量H2O2的作用为 。再加NaOH溶液调节pH在3.7<pH<8.3,目的是 。
(4)向步骤II的滤液中H2O2溶液,再加NaOH溶液调节pH为9,使Mn2+转化成MnO2,在这一过程中H2O2起 (填氧化剂、还原剂)的作用。
(16分)回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由锰粉制取MnO2的步骤和数据如下:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)2 | 8.3 | 9.8 |
(2)步骤I中滤渣的化学式 ,步骤I中滤渣的化学式 。
(3)向步骤I的滤液中加足量H2O2的作用为 。再加NaOH溶液调节pH在3.7<pH<8.3,目的是 。
(4)向步骤II的滤液中H2O2溶液,再加NaOH溶液调节pH为9,使Mn2+转化成MnO2,在这一过程中H2O2起 (填氧化剂、还原剂)的作用。
(16分)回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由锰粉制取MnO2的步骤和数据如下:

|
物质 |
开始沉淀 |
沉淀完全 |
|
Fe(OH)3 |
2.7 |
3.7 |
|
Fe(OH)2 |
7.6 |
9.6 |
|
Fe(OH)2 |
8.3 |
9.8 |
(1)在加热条件下,用浓盐酸浸取锰粉得到含有Mn2+、Fe3+等离子的溶液,MnO2与浓盐酸反应的离子方程式 ,该处理方法的缺点 。
(2)步骤I中滤渣的化学式 ,步骤I中滤渣的化学式 。
(3)向步骤I的滤液中加足量H2O2的作用为 。再加NaOH溶液调节pH在3.7<pH<8.3,目的是 。
(4)向步骤II的滤液中H2O2溶液,再加NaOH溶液调节pH为9,使Mn2+转化成MnO2,在这一过程中H2O2起 (填氧化剂、还原剂)的作用。
回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由锰粉制取MnO2的步骤和数据如下:

| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)2 | 8.3 | 9.8 |
(1)在加热条件下,用浓盐酸浸取锰粉得到含有Mn2+、Fe3+等离子的溶液,MnO2与浓盐酸反应的离子方程式 ,该处理方法的缺点 。
(2)步骤I中滤渣的化学式 ,步骤I中滤渣的化学式 。
(3)向步骤I的滤液中加足量H2O2的作用为 。再加NaOH溶液调节pH在3.7<pH<8.3,目的是 。
(4)向步骤II的滤液中H2O2溶液,再加NaOH溶液调节pH为9,使Mn2+转化成MnO2,在这一过程中H2O2起 (填氧化剂、还原剂)的作用。