题目内容
(2013?浦东新区三模)2004年诺贝尔化学奖授予阿龙?切哈诺沃等三位科学家,以表彰他们发现了泛素调节的蛋白质降解.化合物A是天然蛋白质水解的最终产物,其相对分子质量为165,其中O元素的质量分数小于20%,N元素的质量分数小于10%.
(1)化合物A的分子式为
 .写出A发生缩聚反应的方程式
.写出A发生缩聚反应的方程式
(2)化合物B是A的同分异构体,是某芳香烃一硝化后的唯一产物(硝基连在芳环上).则化合物B的结构简式是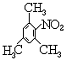
 .
.
写出制备TNT的化学方程式
 .
.
(1)化合物A的分子式为
C9H11O2N
C9H11O2N
;光谱测定显示,化合物A分子结构中不存在甲基(-CH3),则化合物A的结构简式为

n
 +(n-1)H20
+(n-1)H20

| 一定条件 |
 +(n-1)H20
+(n-1)H20n
 +(n-1)H20
+(n-1)H20
.
| 一定条件 |
 +(n-1)H20
+(n-1)H20(2)化合物B是A的同分异构体,是某芳香烃一硝化后的唯一产物(硝基连在芳环上).则化合物B的结构简式是


写出制备TNT的化学方程式


分析:(1)根据含氧量和含氮量推出A含有的官能团;由A是天然蛋白质水解的最终产物,推断A为α-氨基酸,含有一个氨基和羧基;
(2)C9H12芳香烃硝化后只得到一种产物,说明芳香烃的结构的对称性,应为1,3,5-三甲基苯;甲苯甲基邻对位氢原子易被取代,生成2,4,6-三硝基甲苯.
(2)C9H12芳香烃硝化后只得到一种产物,说明芳香烃的结构的对称性,应为1,3,5-三甲基苯;甲苯甲基邻对位氢原子易被取代,生成2,4,6-三硝基甲苯.
解答:解:(1)由A是天然蛋白质水解的最终产物,推断A为α-氨基酸,165×20%=33,故只含有2个氧原子,165×10%=16.5,故只含有1个氮原子原子,即含有一个氨基和羧基,其余为碳和氢元素,165-45-16=104,为8个碳和8个氢原子,A的分子式为C9H11O2N;A是天然蛋白质的水解产物,一定是一种α-氨基酸,光谱测定显示,分子结构中不存在甲基(-CH3),所以是含有苯环的结构,所以结构简式为: ;
; 在一定条件下发生缩聚反应的方程式:n
在一定条件下发生缩聚反应的方程式:n
 +(n-1)H20,
+(n-1)H20,
故答案为:C9H11O2N; ;n
;n
 +(n-1)H20;
+(n-1)H20;
(2)C9H12芳香烃硝化后只得到一种产物,应为1,3,5-三甲基苯,所以B为 ,
,
甲苯中苯环受甲基的影响,在浓硫酸做催化剂、加热条件下,和硝酸易发生取代反应,其中甲苯的甲基邻对位氢原子易被取代,生成2,4,6-三硝基甲苯,该反应为 ,故答案为:
,故答案为: ;
;
 ;
; 在一定条件下发生缩聚反应的方程式:n
在一定条件下发生缩聚反应的方程式:n
| 一定条件 |
 +(n-1)H20,
+(n-1)H20,故答案为:C9H11O2N;
 ;n
;n
| 一定条件 |
 +(n-1)H20;
+(n-1)H20;(2)C9H12芳香烃硝化后只得到一种产物,应为1,3,5-三甲基苯,所以B为
 ,
,甲苯中苯环受甲基的影响,在浓硫酸做催化剂、加热条件下,和硝酸易发生取代反应,其中甲苯的甲基邻对位氢原子易被取代,生成2,4,6-三硝基甲苯,该反应为
 ,故答案为:
,故答案为: ;
;
点评:本题考查有机推断与合成,主要考查学生阅读信息获取知识的能力与思维能力,是对有机化合物知识的综合考查,利用给出的反应信息计算推断A的结构比较麻烦,难度较大.

练习册系列答案
相关题目