题目内容
已知电池总反应为:Zn+2MnO2+H2O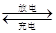 ZnO+2MnO(OH)。下列说法正确的是
ZnO+2MnO(OH)。下列说法正确的是
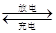 ZnO+2MnO(OH)。下列说法正确的是
ZnO+2MnO(OH)。下列说法正确的是| A.放电时,Zn为负极,ZnO为正极,MnO2为催化剂 |
| B.放电时,该电池的正极反应为:MnO2+e-+H2O=MnO(OH)+OH- |
| C.充电时,电池将化学能转为电能 |
| D.放电时,溶液中的阴离子向原电池的正极移动 |
B
试题分析:放电时,Zn为负极,MnO2为正极,A错误;放电时正极发生还原反应,B正确;充电时电能转变为化学能,C错误;放电时阴离子向负极移动,D错误。答案选B。
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
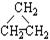 ③CH3CH2CH3 ④HC
③CH3CH2CH3 ④HC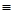 CCH3
CCH3 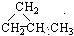 ⑥CH3CH=CHCH3
⑥CH3CH=CHCH3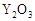 的
的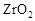 晶体,它在高温下能传导
晶体,它在高温下能传导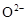 。回答如下问题:①以丁烷(
。回答如下问题:①以丁烷(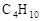 )代表汽油,这个电池放电时发生反应的化学方程式是_________________________________________________________。
)代表汽油,这个电池放电时发生反应的化学方程式是_________________________________________________________。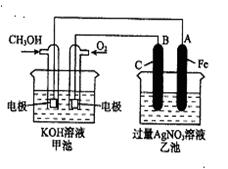

 时发生的化学反应可用下式表示:
时发生的化学反应可用下式表示: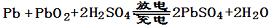
 + 2e – + 4 H+= PbSO4 + 2H2O
+ 2e – + 4 H+= PbSO4 + 2H2O