题目内容
下表中数据是第三周期的三种金属元素X、Y、Z逐渐失去电子的电离能.
试回答下列问题
(1)根据数据分析,X、Y、Z的最外层电子数,简述理由
(2)X元素的原子核外最外层电子排布式为
(3)X、Y、Z三元素的原子半径由大到小顺序为
(4)第三周期中能与Y元素形成YD型化合物的元素D位于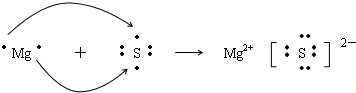
 .
.
(5)写出金属Y与石墨电极、稀硫酸构成的原电池的电极反应式:
负极:
正极:
| 电离能/kJ?mol-1 | |||||||
| X | 578 | 1817 | 2745 | 11575 | 14830 | 18376 | 23293 |
| Y | 738 | 1451 | 7733 | 10540 | 13630 | 17995 | 21703 |
| Z | 496 | 4562 | 6912 | 9943 | 13353 | 16610 | 20114 |
(1)根据数据分析,X、Y、Z的最外层电子数,简述理由
X、Y、Z的最外层电子数分别是3、2、1,由电离能相差很大时较小的电离能即为其最外层电子全失去时的电离能,从而确定其最外层电子数
X、Y、Z的最外层电子数分别是3、2、1,由电离能相差很大时较小的电离能即为其最外层电子全失去时的电离能,从而确定其最外层电子数
.(2)X元素的原子核外最外层电子排布式为
3s23p1
3s23p1
.(3)X、Y、Z三元素的原子半径由大到小顺序为
Z>Y>X(或Na>Mg>Al)
Z>Y>X(或Na>Mg>Al)
;X、Y、Z三元素的离子半径由大到小顺序为Z>Y>X(或Z+>Y2+>X3+或Na+>Mg2+>Al3+)
Z>Y>X(或Z+>Y2+>X3+或Na+>Mg2+>Al3+)
.(4)第三周期中能与Y元素形成YD型化合物的元素D位于
ⅥA
ⅥA
族,用电子式表示化合物YD的形成过程

(5)写出金属Y与石墨电极、稀硫酸构成的原电池的电极反应式:
负极:
Mg-2e-═Mg2+
Mg-2e-═Mg2+
正极:
2H++2e-═H2↑
2H++2e-═H2↑
.分析:(1)根据图表分析,电离能相差很大时较小的电离能即为其最外层电子全失去时的电离能,从而确定其最外层电子数;
(2)根据能量最低原理书写电子排布式;
(3)根据元素周期律判断原子半径、离子半径大小;
(4)根据化合价判断所属主族;根据得失电子写出形成过程;
(5)镁、石墨电极、稀硫酸构成原电池,活泼金属镁作负极,石墨作正极,负极上失电子生成离子进入溶液,正极上氢离子得电子生成氢气.
(2)根据能量最低原理书写电子排布式;
(3)根据元素周期律判断原子半径、离子半径大小;
(4)根据化合价判断所属主族;根据得失电子写出形成过程;
(5)镁、石墨电极、稀硫酸构成原电池,活泼金属镁作负极,石墨作正极,负极上失电子生成离子进入溶液,正极上氢离子得电子生成氢气.
解答:解:(1)由上述数据可以看出,X元素第一、二、三电离能相差不大,但第三、四电离能差距很大,故X元素的原子最外层电子数为为3(为铝原子),
Y元素的一、二电离能相差不大,第二、三电离能差距很大,故Y元素的原子最外层电子数为2(为镁原子),
Z元素的第一电离能和第二电离能相对差距很大,其他电离能差距不大,故Z元素的原子最外层电子数为1(为钠元素),
故答案为:X、Y、Z的最外层电子数分别是3、2、1,由电离能相差很大时较小的电离能即为其最外层电子全失去时的电离能,从而确定其最外层电子数;
(2)X为铝元素,根据能量最低原理书写电子排布式为1S2 2S22P63s23p1,其最外层是M层,M层上S能级最多排2个电子,P能级排1个电子,所以X元素的原子核外最外层电子排布式为3s23p1,故答案为:3s23p1;
(3)由元素周期律知,同一周期元素,原子半径随着原子序数的增大而减小,所以X、Y、Z三元素的原子半径由大到小顺序为Z>Y>X(或Na>Mg>Al);具有相同电子层结构的离子其离子半径随着原子序数的增大而减小,所以X、Y、Z三元素的离子半径由大到小顺序为Z>Y>X(或Z+>Y2+>X3+或Na+>Mg2+>Al3+),
故答案为:Z>Y>X(或Na>Mg>Al);Z>Y>X(或Z+>Y2+>X3+或Na+>Mg2+>Al3+);
(4)在YD中,Y是镁元素,显+2价,根据化合物中各元素的化合价的代数和为0,所以D显-2价;主族元素中,最低负价的绝对值+最高正价=8,所以最高正价为+6价,最高正价序数=其最外层电子数,结合题意知,D是硫元素,在ⅥA族;硫化镁是离子化合物,镁原子失去2个电子生成镁离子,硫原子得电子生成硫离子,其形成过程为:
 ,
,
故答案为:ⅥA; ;
;
(5)镁、石墨电极、稀硫酸构成原电池,活泼金属镁作负极,石墨作正极,负极上失电子生成离子进入溶液,正极上氢离子得电子生成氢气,所以负极上电极反应式为:Mg-2e-═Mg2+,正极上电极反应式为:2H++2e-═H2↑,
故答案为:Mg-2e-═Mg2+;2H++2e-═H2↑.
Y元素的一、二电离能相差不大,第二、三电离能差距很大,故Y元素的原子最外层电子数为2(为镁原子),
Z元素的第一电离能和第二电离能相对差距很大,其他电离能差距不大,故Z元素的原子最外层电子数为1(为钠元素),
故答案为:X、Y、Z的最外层电子数分别是3、2、1,由电离能相差很大时较小的电离能即为其最外层电子全失去时的电离能,从而确定其最外层电子数;
(2)X为铝元素,根据能量最低原理书写电子排布式为1S2 2S22P63s23p1,其最外层是M层,M层上S能级最多排2个电子,P能级排1个电子,所以X元素的原子核外最外层电子排布式为3s23p1,故答案为:3s23p1;
(3)由元素周期律知,同一周期元素,原子半径随着原子序数的增大而减小,所以X、Y、Z三元素的原子半径由大到小顺序为Z>Y>X(或Na>Mg>Al);具有相同电子层结构的离子其离子半径随着原子序数的增大而减小,所以X、Y、Z三元素的离子半径由大到小顺序为Z>Y>X(或Z+>Y2+>X3+或Na+>Mg2+>Al3+),
故答案为:Z>Y>X(或Na>Mg>Al);Z>Y>X(或Z+>Y2+>X3+或Na+>Mg2+>Al3+);
(4)在YD中,Y是镁元素,显+2价,根据化合物中各元素的化合价的代数和为0,所以D显-2价;主族元素中,最低负价的绝对值+最高正价=8,所以最高正价为+6价,最高正价序数=其最外层电子数,结合题意知,D是硫元素,在ⅥA族;硫化镁是离子化合物,镁原子失去2个电子生成镁离子,硫原子得电子生成硫离子,其形成过程为:
 ,
,故答案为:ⅥA;
 ;
;(5)镁、石墨电极、稀硫酸构成原电池,活泼金属镁作负极,石墨作正极,负极上失电子生成离子进入溶液,正极上氢离子得电子生成氢气,所以负极上电极反应式为:Mg-2e-═Mg2+,正极上电极反应式为:2H++2e-═H2↑,
故答案为:Mg-2e-═Mg2+;2H++2e-═H2↑.
点评:本题考查了微粒半径的比较、电负性、原电池原料等知识点,属综合题,难度不大,注意离子化合物和共价化合物形成过程的区别.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
下表中数据是第三周期的三种金属元素X、Y、Z逐渐失去电子的电离能.
试回答下列问题
(1)根据数据分析,X、Y、Z的最外层电子数,简述理由______.
(2)X元素的原子核外最外层电子排布式为______.
(3)X、Y、Z三元素的原子半径由大到小顺序为______;X、Y、Z三元素的离子半径由大到小顺序为______.
(4)第三周期中能与Y元素形成YD型化合物的元素D位于______族,用电子式表示化合物YD的形成过程______.
(5)写出金属Y与石墨电极、稀硫酸构成的原电池的电极反应式:
负极:______
正极:______.
| 电离能/kJ?mol-1 | |||||||
| X | 578 | 1817 | 2745 | 11575 | 14830 | 18376 | 23293 |
| Y | 738 | 1451 | 7733 | 10540 | 13630 | 17995 | 21703 |
| Z | 496 | 4562 | 6912 | 9943 | 13353 | 16610 | 20114 |
(1)根据数据分析,X、Y、Z的最外层电子数,简述理由______.
(2)X元素的原子核外最外层电子排布式为______.
(3)X、Y、Z三元素的原子半径由大到小顺序为______;X、Y、Z三元素的离子半径由大到小顺序为______.
(4)第三周期中能与Y元素形成YD型化合物的元素D位于______族,用电子式表示化合物YD的形成过程______.
(5)写出金属Y与石墨电极、稀硫酸构成的原电池的电极反应式:
负极:______
正极:______.