题目内容
【题目】下列物质在水溶液中的电离方程式书写正确的是
A.KClO3=K++3O2—+Cl5+B.NaHSO4= Na++HSO4—
C.H2SO4=H++ SO42—D.Al2(SO4)3= 2Al3++3SO42—
【答案】D
【解析】考查电离方程式的正误判断。A、B、C都是不正确的,分别应该是KClO3=K++ClO3-、NaHSO4=Na++H++SO42-、H2SO4=2H++SO42-。所以的正确答案选D。

 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案【题目】根据实验操作,实验现象和所得出的结论不正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 取一小块镁带和一小片铝,用砂纸磨去表面的氧化膜,分别放入两支试管,再各加入同浓度同体积的盐酸 | 镁比铝产生气泡速率更快 | 金属性:Mg>Al |
B | 向某无色溶液中加入铜片和稀硫酸 | 试管口产生红棕色气体 | 该无色溶液中含有NO |
C | 向淀粉KI溶液中滴入3滴稀盐酸,再加入10%的H2O2溶液 | 滴入稀盐酸未见溶液变蓝;加入H2O2溶液后,溶液立即变蓝 | 酸性条件下,H2O2氧化性强于I2 |
D | 取少量白色晶体于试管,加入氢氧化钠溶液并加热 | 试管口湿润蓝色石蕊试纸变红 | 白色晶体一定含有NH4+ |
A. AB. BC. CD. D
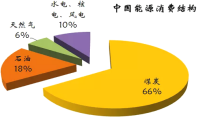
【题目】下图为我国目前的能源消费结构图:
(1)由图中数据可知,一定时期内,我国的能源结构仍以煤碳为主,但直接燃烧煤炭的弊端是____。
(2)将煤转化为水煤气可有效降低煤对环境的破坏性,能量变化如图所示:
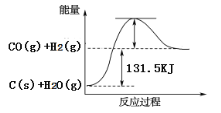
根据以上数据,写出该反应的热化学方程式_________________;
(3)甲醇是重要的化学工业基础原料和清洁液体燃料。将煤液化将克服直接将煤作为燃料的不足。其反应原理为CO2(g)+3H2(g)![]() CH3OH(g) +H2O(g)。
CH3OH(g) +H2O(g)。
①在适当的催化剂作用下,该反应能自发进行。则该反应ΔH______0(填“>”、“<”或“=”)
②在体积一定的密闭容器中发生该反应,达到平衡后升高温度,下列说法正确的是______。
A.平衡正向移动 B.达到新的平衡后体系的压强增大
C.H2的转化率增大 D.体系的密度增大
③下列叙述能说明此反应达到平衡状态的是_______。(填字母)
a.混合气体的平均相对分子质量保持不变 b.1 mol CO2生成的同时有3 mol H—H键断裂
c.CO2的转化率和H2的转化率相等 d.混合气体的密度保持不变
④在相同起始温度(500℃)、起始体积相同(2L)的三个密闭容器中分别进行该反应,控制不同条件,反应过程中部分数据见下表:
反应时间 | CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
反应Ⅰ:恒温恒容 | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
反应Ⅱ:恒温恒压 | 0 min | 1 | 3 | 1 | 1 |
反应Ⅲ:绝热恒容 | 0 min | 0 | 0 | 2 | 2 |
查阅资料发现500℃时该反应的平衡常数为2.5。则反应Ⅰ在10min时v正______v逆,则反应均达到平衡时,反应Ⅰ、Ⅱ对比H2的百分含量关系w%Ⅰ(H2)______w%Ⅱ(H2),反应Ⅰ、Ⅲ对比:平衡时CH3OH的浓度c(I)_______c(Ⅲ)(本小题均用“>”、“<”或“=”填空)。