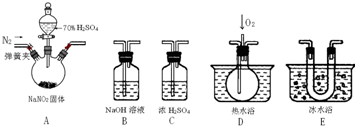
题目内容
已知:NO+NO2+2NaOH====2NaNO2+H2O,2NO2+2NaOH====NaNO3+NaNO2+H2O。NO和NO2的混合气体的组成可表示为NOx。该混合气体通入NaOH溶液被完全吸收时,x的值为( )
A.x≤1.5 B.x=3.5 C.x=1.2 D.x≥1.5
D
解析:由题中所给反应过程可知,要使混合气体通入NaOH溶液被完全吸收,则NO2与NO的物质的量比应大于等于1,即n(NO2)/n(NO)≥1。当n(NO2)/n(NO)=1时,混合气体中所含NO2和NO的物质的量相等,此时x=1.5,若要n(NO2)/n(NO)>1,须x>1.5,故x应满足的条件是x≥1.5。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
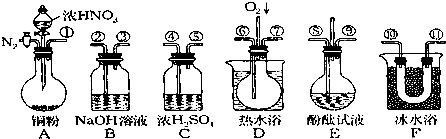
 某同学用下面装置实现铜与浓、稀硝酸反应,过程如下:
某同学用下面装置实现铜与浓、稀硝酸反应,过程如下: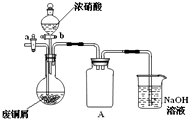 碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下: