题目内容
【题目】电石广泛用于生产PVC、维尼纶等,电石与水反应所得残渣——电石渣,主要含Ca(OH)2、CaCO3及少量其他杂质。某工业电石渣的几种回收利用流程如下:
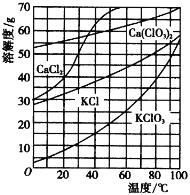
几种物质在水中的溶解度曲线如右图。回答下列问题:
(1)常温氯化
①反应的化学方程式是 。
②提高Cl2转化为Ca(ClO)2的转化率可行的措施有_______(填序号)。
A.加热升高温度 B.适当减缓通入Cl2速率
C.充分搅拌浆料 D.加水使Ca(OH)2完全溶解
③电石渣中的有害杂质CN-与ClO-反应转化为两种无害的气体,每转化1 mol CN-至少需要消耗氧化剂ClO-_______mol。
(2)75 ℃氯化
①生成氯酸钙中氯的化合价为 ,氯化完成后过滤,滤渣的主要成分为______(填化学式)。
②氯酸钙能与KCl反应转化为氯酸钾的原因是 。
(3)有机反应
首先生成氯代乙醇,其结构简式为 ,氯代乙醇再与Ca(OH)2反应生产环氧乙烷。总反应的化学方程式是 。
【答案】
(1)①2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O;②BC;③2.5;
(2)①+5价;CaCO3、Ca(OH)2;
②75℃,氯酸钾的溶解度比氯酸钙、氯化钾、氯化钙都小得多;
(3)ClCH2CH2OH;CH2=CH2+Cl2+Ca(OH)2—→![]() +CaCl2+H2O;
+CaCl2+H2O;
【解析】
试题分析:(1)①常温氯化是氯气与氢氧化钙的反应,反应的化学方程式为2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O;
②A.加热升高温度,可以提高反应速率,但不能改变原料转化率,错误;B.适当减缓通入Cl2速率,有利于反应充分进行,可以提高原料利用率,正确;C.充分搅拌浆料,有利于反应充分进行,可以提高原料利用率,正确;D.加水使Ca(OH)2完全溶解,反应速率减慢,但不能改变原料转化率,错误;故选BC;
③电石渣中的有害杂质CN-与ClO-反应转化为两种无害的气体,两种气体为二氧化碳和氮气,该反应方程式为2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH-,消耗1molCN-转移5mol电子,至少需要消耗氧化剂ClO-的物质的量为![]() =2.5mol,故答案为:2.5;
=2.5mol,故答案为:2.5;
(2)①氯酸钙[Ca(ClO3)2]中氯的化合价为+5价,氯化完成后过滤,碳酸钙难溶于水,氢氧化钙微溶于水,因此滤渣的主要成分为CaCO3、Ca(OH)2,故答案为:+5价;CaCO3、Ca(OH)2;
②根据溶解度曲线可知,75 ℃,氯酸钾的溶解度比氯酸钙、氯化钾、氯化钙都小得多,使得氯酸钙能与KCl反应转化为氯酸钾,故答案为:75 ℃,氯酸钾的溶解度比氯酸钙、氯化钾、氯化钙都小得多;
(3)氯代乙醇的结构简式为ClCH2CH2OH,氯代乙醇再与Ca(OH)2反应生产环氧乙烷,反应的化学方程式为CH2=CH2+Cl2+Ca(OH)2—→![]() +CaCl2+H2O,故答案为:CH2=CH2+Cl2+Ca(OH)2—→
+CaCl2+H2O,故答案为:CH2=CH2+Cl2+Ca(OH)2—→![]() +CaCl2+H2O。
+CaCl2+H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案