题目内容
【题目】现有73g氯化氢(HCl)气体,则:
(1)该气体的摩尔质量为_____________。
(2)该气体的物质的量为________ ,所含分子总数为___________________个。
(3)该气体在标准状况下的体积为_____________L。
(4)将73g氯化氢(HCl)气体溶于水配成2L溶液,所得盐酸的物质的量浓度为__________。
(5)在标准状况下,测得1.92g某气体的体积为672ml,计算此气体的相对分子质量__________。
(6)N2、CO2、SO2三种气体的质量比为7:11:16时,它们的分子个数比为_______,同温同压下体积比为___________。
【答案】36.5g/mol2 mol2NA(1.204![]() 1024)44.81mol/L641:1:11:1:1
1024)44.81mol/L641:1:11:1:1
【解析】
(1)HCl气体的相对分子质量是36.5,则该气体的摩尔质量为36.5g/mol;
(2)根据n=![]() 可知该气体的物质的量为
可知该气体的物质的量为![]() =2mol,所含分子总数为2NA个;
=2mol,所含分子总数为2NA个;
(3)准状况下气体的摩尔体积是22.4L/mol,所以该气体在标准状況下的体积为2mol×22.4L/mol=44.8L;
(4)将73g氯化氢(HCl)气体的物质的量为2mol,溶于水配成2L溶液,所得盐酸的物质的量浓度为![]() ;
;
(5)在标准状況下,测得1.92g某气体的体积为672mL,物质的量是![]() =0.03mol,所以此气体的相对分子质量为
=0.03mol,所以此气体的相对分子质量为![]() =64;
=64;
(6)N2、CO2、SO2三种气体的质量比为7:11:16时,它们的分子个数比为:![]() =1:1:1,则物质的量之比为1:1:1,同温同压下体积比为1:1:1。
=1:1:1,则物质的量之比为1:1:1,同温同压下体积比为1:1:1。

 名校课堂系列答案
名校课堂系列答案【题目】氨基磺酸镍[Ni(H2NSO3)2]是工业电镀镍所必需的化工原料,某科研小组先用尿素、SO3合成中间体氨基磺酸(H2NSO3H),再用氨基磺酸、金属镍和双氧水反应来合成氨基磺酸镍。已知磺化制氨基磺酸反应原理和整个过程的流程图如下:
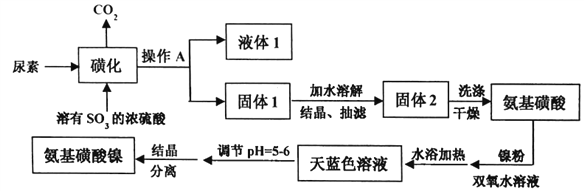
①CO(NH2)2(s)+SO3(g)→H2NCONHSO3H(s) △H<0
②H2NCONHSO3H (s)+ H2SO4→2H2NSO3H (s)+ CO2↑
已知物质的部分性质如下:
物质 | 溶解性 | 稳定性 | 酸碱性 |
氨基磺酸 | 溶于水、不溶于乙醇 | pH较低时发生水解生成NH4HSO4 | 强酸性 |
氨基磺酸镍 | 溶于水、乙醇 | 高于110℃时分解 | 酸性 |
请回答
(1)操作A的名称是_________液体1的主要成分是_______(填化学式)。
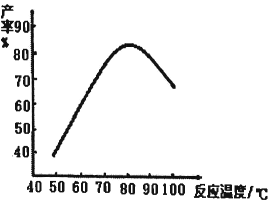
(2)“磺化”过程的温度与产率的关系如下图。温度高于80℃时氨基磺酸的产率会降低,原因一是升高温度平衡逆向移动,原因二是__________。
(3)写出制备氨基磺酸镍的化学方程式____________________。
(4)写出固体2洗涤的操作过程___________________。
(5)流程图中“天蓝色溶液”需要调节pH=5~6的原因是___________。