题目内容
【题目】在一定条件下,1mol N2和3mol H2混合后反应,达到平衡时测得混合气体的密度是同温同压下氢气的5倍,则氮气的转化率为( )
A. 20% B. 30% C. 40% D. 50%
【答案】B
【解析】达到平衡时测得混合气体的密度是同温同压下氢气的5倍,则平衡时混合气体平衡摩尔质量为5×2g/mol=10g/mol,混合气体总质量=1mol×28g/mol+3mol×2g/mol=34g,则平衡时混合气体总物质的量为![]() =3.4mol,设参加反应的氮气物质的量为x,则:
=3.4mol,设参加反应的氮气物质的量为x,则:
N2+3 H2=2 NH3 物质的量减小
1mol 2mol
x 1mol+3mol-3.4mol=0.6mol
所以x=![]() =0.3mol,故氮的转化率为
=0.3mol,故氮的转化率为![]() ×100%=30%,故选B。
×100%=30%,故选B。

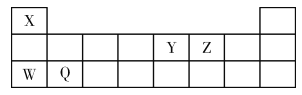
【题目】X、Y、Z、M、W、Q、R是7种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | W | Q | R |
原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
主要化合价 | +1 | +3 | +6,﹣2 | +7,﹣1 | +5,﹣3 | ﹣2 | +1 |
完成下列填空:
(1)上述元素中,金属性最强的在周期表中的位置是________________________________;X、Y、Q各自形成的简单离子中,离子半径由大到小的顺序是_______(填离子符号)。
W和R按原子个数比1﹕4构成的阳离子所含的化学键是____________________。
(2)表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是_______(填化学
式),其电离方程式为_____________________________________。
(3)M与Z相比,非金属性较强的是_____________(填元素名称),请从原子结构的角度说明理由_________________________________________________________________。
(4)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下:
![]() KMnO4+
KMnO4+![]() H2O2+
H2O2+![]() H2SO4 →
H2SO4 → ![]() K2SO4+
K2SO4+![]() MnSO4+
MnSO4+![]() O2↑+
O2↑+![]() H2O
H2O
请配平,当有0.5 mol H2O2参加此反应,电子转移的个数为______________________。