题目内容
10.Mg和SiO2在高温下反应生成MgO和Mg2Si.下列说法正确的是( )| A. | 微粒的半径:Si>Mg | B. | 氧元素不存在同素异形体 | ||
| C. | Mg的还原性强于Si | D. | 该反应是置换反应,镁元素被氧化 |
分析 A.同周期从左到右原子半径依次减小;
B.氧元素有两种单质;
C.同周期从左到右单质的还原性减弱;
D.一种单质与一种化合物反应生成另一种单质和另一种化合物的反应叫置换反应.
解答 解:A.同周期从左到右原子半径依次减小,则微粒的半径:Si<Mg,故A错误;
B.氧元素有两种单质,氧气和臭氧,则氧元素存在同素异形体,故B错误;
C.同周期从左到右单质的还原性减弱,则Mg的还原性强于Si,故C正确;
D.一种单质与一种化合物反应生成另一种单质和另一种化合物的反应叫置换反应,该反应中生成物中没有单质,所以不是置换反应,故D错误.
故选C.
点评 本题考查了同周期元素性质的递变规律、置换反应的概念等,题目难度不大,侧重于基础知识的考查.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.下列说法正确的是( )
| A. | 氯气有毒,所以不能用氯气对自来水进行消毒 | |
| B. | 液氯是纯净物,而氯水是混合物 | |
| C. | 碘化钾水溶液能使淀粉变蓝 | |
| D. | 在一个反应中,氧化剂和还原剂不可能是同一物质 |
5. 向盛有100mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示.则原HCl物质的量浓度是( )
向盛有100mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示.则原HCl物质的量浓度是( )
 向盛有100mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示.则原HCl物质的量浓度是( )
向盛有100mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示.则原HCl物质的量浓度是( )| A. | 4mol/L | B. | 3mol/L | C. | 2mol/L | D. | 1mol/L |
15.一种石墨烯锂硫电池(2Li+S8═Li2S8)工作原理示意如图.下列有关该电池说法正确的是( )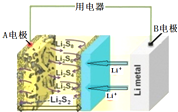

| A. | B电极发生还原反应 | |
| B. | A电极上发生的一个电极反应为:2Li++S8+2e-═Li2S8 | |
| C. | 每生成1mol Li2S8转移0.25mol电子 | |
| D. | 电子从B电极经过外电路流向A电极,再经过电解质流回B电极 |
20.下列说法正确的是( )
| A. | 升高温度均可以使氨水、氯化铵溶液中c(NH4+)增大 | |
| B. | H2O是一种弱电解质 | |
| C. | 用托盘天平称量NaOH固体时,需在左右托盘上各方一块质量相等的滤纸 | |
| D. | 用25mL滴定管量取25.00mLNaOH溶液时,需将调好零点的滴定管中所有液体放出 |
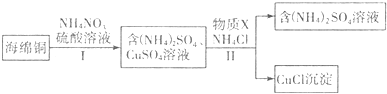
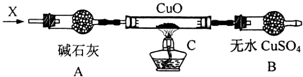 铜是常见的变价金属.为了比较正一价铜和正二价铜的稳定性,并研究氧化铜的氧化性,某化学小组的同学进行了以下实验.
铜是常见的变价金属.为了比较正一价铜和正二价铜的稳定性,并研究氧化铜的氧化性,某化学小组的同学进行了以下实验.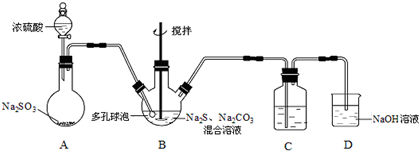
 燃煤厂为减少SO2的排放,可采取的措施是:
燃煤厂为减少SO2的排放,可采取的措施是: