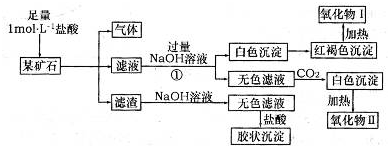
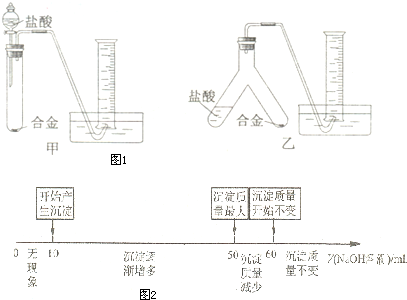
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图1所示装置进行有关实验.
已知:①SO
2难溶于饱和亚硫酸氢钠溶液.②SO
2能与酸性高锰酸钾溶液发生氧化还原反应.
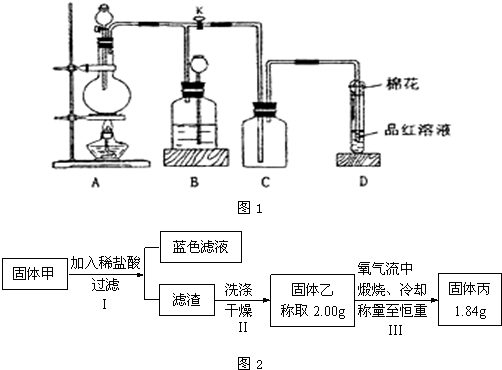
请回答:
(1)装置A中发生的化学反应方程式为______.此反应表明浓硫酸具有(填字母)______.
a.酸性b.脱水性c.强氧化性d.吸水性
(2)装置D中试管口放置的棉花中浸入______溶液,其作用是______.
(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中的现象是______.B中应放置的液体是(填字母)______.
a.水b.饱和NaHSO
3溶液c.酸性KMnO
4溶液d.NaOH溶液
(4)实验中,取一定质量的铜片和一定体积18.4mol?L
-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①有一定量的余酸但未能使铜片完全溶解,你认为原因是______.
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是(填字母)______.
a.银粉b.铁粉c.BaCl
2溶液d.NaHCO
3溶液
(5)实验中发现试管内除了产生白色固体外,在铜表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜.
查阅资料:
i.氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu
2+和铜单质,在氧气流中煅烧,可以转化为氧化铜.
ii.硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图2所示实验:
①Ⅲ中在煅烧过程中一定发生的反应的化学方程式为______.
②下列对于固体甲的成分的判断中,正确的是(填字母选项)______.
a.固体甲中,CuO和Cu
2O至少有一种
b.固体甲中,CuS和Cu
2S不能同时存在
c.固体甲中若没有Cu
2O,则一定有Cu
2S
d.固体甲中若存在Cu
2O,也可能有Cu
2S.