题目内容
全世界每年被腐蚀损耗的钢铁量非常惊人,在潮湿空气中发生吸氧腐蚀是钢铁腐蚀的主要原因。
(1)在潮湿空气中,钢铁发生吸氧腐蚀时的负极反应的电极反应式为 。
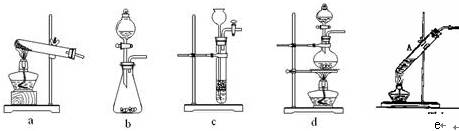
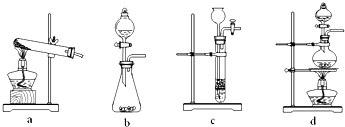
(2)已知草酸(H2C2O4)分解的化学方程式为:H2C2O4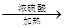 CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 (填答案编号)。
CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 (填答案编号)。

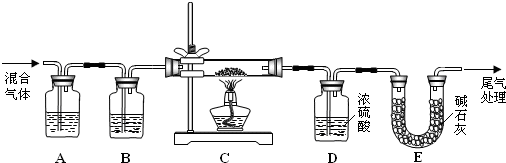
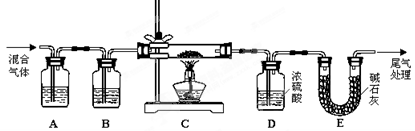
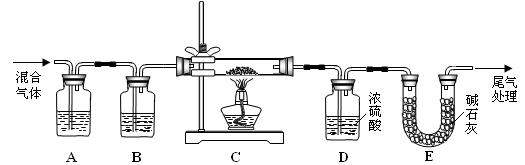
(3)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3·nH2O和Fe两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
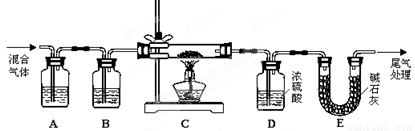
①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次可能是 、 (填答案编号)。
a. 浓硫酸 b.澄清的石灰水 c. 氢氧化钠溶液 d. 无水氯化钙
②E装置的作用是 ,
上述装置最后尾气处理的方法是 。
③准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32 g,D中浓硫酸增重0.72 g,则n = 。
④在本实验中,下列情况会使测定结果n偏大的是 (填答案编号)。
a.缺少装置B b.缺少装置E c.反应后的固体中有少量Fe2O3·nH2O
(14分)(1)Fe-2e-==Fe2+ (2分) (2)d (2分) (3)①c,a(2分)
②防止空气中的CO2和H2O进入体系,影响实验结果,(2分) 点燃(2分)③2 (2分) ④ab(2分)
【解析】
试题分析:(1)在潮湿空气中,钢铁发生吸氧腐蚀时,铁是负极,失去电子,则负极反应的电极反应式为Fe-2e-==Fe2+。
(2)醋酸是液体,a不正确。反应需要加热,则bc不正确,所以正确的答案选d。
(3)①由于生成的CO中混有CO2,所以必须首先除去CO2,最后在通过浓硫酸干燥,答案选ca。
②由于空气中也含有水蒸气和CO2,所以E装置的作用是防止空气中的CO2和H2O进入体系,影响实验结果。CO属于可燃性气体,所以最后尾气处理的方法是点燃。
③D中浓硫酸增重0.72 g,则生成的水是0.72g,物质的量是0.04mol。硬质玻璃管中剩余固体质量为8.32 g,所以固体减少的质量是10.00g-8.32g=1.68g,所以与铁结合的氧原子的质量是1.68g-0.72g=0.96g,物质的量是0.06mol,因此氧化铁的物质的量是0.02mol,则0.02nmol=0.04mol,解得n=2。
④如果少装置B,则D中增加的质量偏高,所以测定结果偏高。同样分析可知,如果缺少E装置,D中增加的质量偏高,所以测定结果偏高。如果反应后的固体中有少量Fe2O3·nH2O,则D中增加的质量减少,测定结果偏低,答案选ab。
考点:考查钢铁的吸氧腐蚀、CO的制备、尾气处理以及有关计算和误差分析
点评:该题是高考中的常见题型,难度大,对学生的要求高。试题在注重对基础知识巩固和训练的同时,侧重对硝酸能力的培养和解题方法的指导与训练,有利于培养学生规范严谨的实验设计能力以及评价能力。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案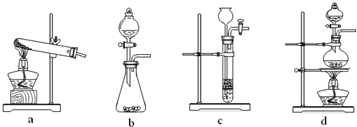
 CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 (填答案编号)。
CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 (填答案编号)。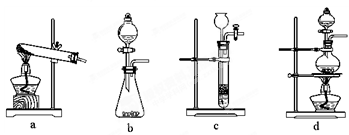
 CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 ▲ 。(填字母)
CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 ▲ 。(填字母)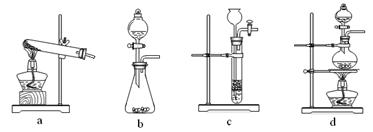
 进行的操作是:(a)检查装置气密性;(b) ▲ 。
进行的操作是:(a)检查装置气密性;(b) ▲ 。 CO↑ + CO2↑ + H2O,
CO↑ + CO2↑ + H2O,