题目内容
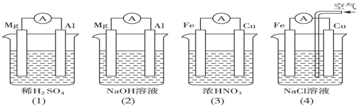
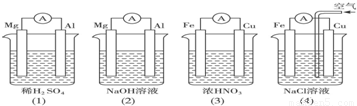
分析如图所示的四个装置,结论正确的是( )
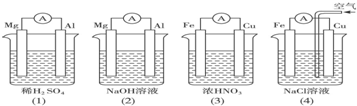

| A.(1)(2)中Mg作负极,(3)(4)中Fe作负极 |
| B.(2)中Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2↑ |
| C.四个装置中某一电极上均有气泡产生 |
| D.(4)中Cu作正极,电极反应式为2H++2e-=H2↑ |
A.(2)中Mg不与NaOH溶液反应,Mg作负极,(3)中因为常温下,Fe被浓硝酸钝化,Cu作负极,故A错误;
B.当NaOH是电解质溶液时,Al作负极(Mg不与NaOH溶液反应),Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2↑,故B正确;
C.(4)中正极反应式为2H2O+O2+4e-=4OH-,负极反应式为Fe-2e-=Fe2+,没有气泡产生,故C错误;
D.(4)中Cu作正极,发生吸氧腐蚀,正极反应式为:2H2O+O2+4e-=4OH-,故D错误.
故选B.
B.当NaOH是电解质溶液时,Al作负极(Mg不与NaOH溶液反应),Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2↑,故B正确;
C.(4)中正极反应式为2H2O+O2+4e-=4OH-,负极反应式为Fe-2e-=Fe2+,没有气泡产生,故C错误;
D.(4)中Cu作正极,发生吸氧腐蚀,正极反应式为:2H2O+O2+4e-=4OH-,故D错误.
故选B.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
 分析如图所示的四个原电池装置,其中结论正确的是( )
分析如图所示的四个原电池装置,其中结论正确的是( )