题目内容
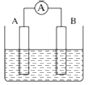
【题目】钴(Co)与钛(Ti)是均可与强酸发生反应的金属。利用电解原理电解CoCl2溶液制取钴,工作原理如图所示,其中Ti-Ru为惰性电极。下列说法正确的是

A. 电解时控制CoCl2溶液的pH在0~1范围内
B. 电解过程中Cl在Ti电极放电生成氯气
C. Ti-Ru的作用是作为损耗阳极材料和传递电流
D. 用CoSO4代替CoCl2会使钴的产率降低
【答案】D
【解析】
根据题意可知,Ti为活泼金属需与电源负极相连,做电解池的阴极,Co2+在阴极得到电子得到Co,Ti-Ru电极上Cl发生失电子的氧化反应,为电解池的阳极,据此分析作答。
根据上述分析可知,
A. Co能与强酸反应产生H2,则电解时不适宜控制CoCl2溶液的pH在强酸性范围内,A项错误;
B. 电解过程中Cl在Ti-Ru电极放电生成氯气,B项错误;
C. Ti-Ru电极为惰性电极,不被损耗,C项错误;
D. 用CoSO4代替CoCl2,则阳极上为OH-放电,使溶液的pH降低,Co可与强酸反应,导致产率降低,D项正确;
答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目