题目内容
【题目】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业,是难溶于水的白色固体,能溶解于硝酸,在潮湿空气中可被迅速氧化。
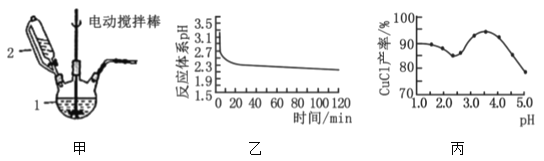
Ⅰ.实验室用CuSO4—NaCl混合液与Na2SO3溶液反应制取CuCl。相关装置及数据如图。
回答以下问题:
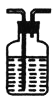
(1)甲图中仪器1的名称是___;制备过程中Na2SO3过量会发生副反应生成[Cu(SO3)2]3-,为提高产率,仪器2中所加试剂应为___。
(2)乙图是体系pH随时间变化关系图,写出制备CuCl的离子方程式___。丙图是产率随pH变化关系图,实验过程中往往用Na2SO3—Na2CO3混合溶液代替Na2SO3溶液,其中Na2SO3的作用是___并维持pH在___左右以保证较高产率。
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是___。
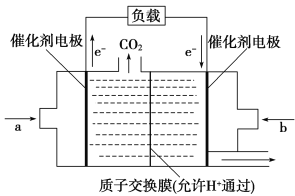
Ⅱ.工业上常用CuCl作O2、CO的吸收剂,某同学利用如图所示装置模拟工业上测定高炉煤气中CO、CO2、N2和O2的含量。
A. | B. |
C. | D. |
已知:Na2S2O4和KOH的混合溶液可吸收氧气。
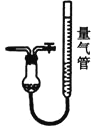
(4)装置A中用盐酸而不能用硝酸,其原因是___(用化学方程式表示)。用D装置测N2含量,读数时应注意___。整套实验装置的连接顺序应为___→D。
【答案】三颈烧瓶 Na2SO3溶液 2Cu2++SO32-+2Cl-+H2O=2CuCl↓+2H++SO42- 与H+作用,调整pH 3.5 洗去晶体表面的杂质离子,同时防止CuCl被氧化 6CuCl+8HNO3=3Cu(NO3)2+3CuCl2+2NO↑+4H2O(或3CuCl+7HNO3=3Cu(NO3)2+3HCl+NO↑+2H2O) 温度降到常温,上下调节量气管至左、右液面相平,该数时视线与凹液面最低处相切 C→B→A
【解析】
(1)根据仪器1的图示解答;制备过程中Na2SO3过量会发生副反应生成[Cu(SO3)2]3- ,需要控制Na2SO3的加入量,据此分析判断;
(2)根据题意,在CuSO4液中加入一定量的Na2SO3和NaCl溶液生成CuCl沉淀,同时溶液的酸性增强,结合Na2CO3的性质分析解答;
(3)根据“氯化亚铜(CuCl)在潮湿空气中可被迅速氧化”分析解答;
(4)根据氯化亚铜(CuCl)能溶解于硝酸 ,结合硝酸的强氧化性书写反应的方程式;根据正确的读数方法解答;用CuCl作O2、CO的吸收剂,测定高炉煤气中CO、CO2、N2和O2的含量,可用KOH吸收二氧化碳,然后用B吸收氧气,再用A吸收CO ,最后用排水法测量氮气的体积,据此分析解答。
(1)甲图中仪器1为三颈烧瓶;制备过程中Na2SO3过量会发生副反应生成[Cu(SO3)2]3- ,为提高产率,可控制Na2SO3的加入量,则仪器2中所加试剂应为Na2SO3溶液;
(2)在提纯后的CuSO4液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl(氯化亚铜)沉淀,同时溶液的酸性增强,生成硫酸,反应的离子方程式为: 2Cu2++SO32-+2Cl-+H2O=2CuCl↓+2H++SO42-,用Na2SO3-Na2CO3混合溶液代替Na2SO3溶液,Na2CO3可与生成的H+反应,及时除去系统中反应生成的H+,利于反应进行,由图象可知,应维持pH在3.5左右;
(3)用去氧水作洗涤剂洗涤产品,可洗去晶体表面的杂质离子,同时防止CuCl被氧化;
(4)根据题意,氯化亚铜(CuCl)能溶解于硝酸,反应的方程式为6CuCl+8HNO3=3Cu(NO3)2+3CuCl2+2NO↑+4H2O(或3CuCl+7HNO3=3Cu(NO3)2+3HCl+NO↑+2H2O);用D装置测N2含量,应注意温度在常温,且左右液面相平,读数时视线与凹液面最低处水平相切,以减小实验误差;用CuCl作O2、CO的吸收剂,测定高炉煤气中CO、CO2、 N2和O2的含量,可用KOH吸收二氧化碳,然后用B吸收氧气,再用A吸收CO,最后用排水法测量氮气的体积,则顺序为C-B-A-D。

 名校课堂系列答案
名校课堂系列答案