题目内容
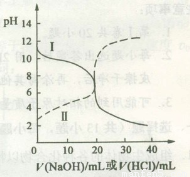
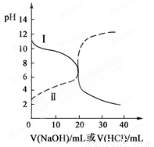
25℃时,取浓度均为0.1 mol/L的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol/LNaOH溶液、0.1 mol/L盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。下列说法正确的是(? )
A.曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.曲线Ⅰ:滴加溶液到20 mL时:??? c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+)
D.曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
D
【解析】
试题分析:由图像可知曲线Ⅰ为HCl滴定氨水的pH变化情况,曲线Ⅱ为NaOH溶液滴定醋酸溶液的pH变化情况。A.C错误。B. 曲线Ⅰ滴加溶液到10 mL时得到的溶液为NH4Cl、NH3·H2O等浓度等体积混合。由于NH3·H2O的电离作用大于NH4+的水解作用,所以溶液中各种离子的浓度关系为c(NH4+)>c(Cl-)>c(OH-)>c(H+);当滴加溶液到20 mL时得到的溶液为NH4Cl溶液。由于存在NH4+的水解作用,所以c(Cl-)>c(NH4+),水解消耗OH-,使的溶液中的H+的浓度大于OH-的浓度。所以c(H+)>c(OH-)。此时该溶液中各种离子的浓度关系为c(Cl-)>c(NH4+)>c c(H+)>(OH-)。错误。D. 曲线Ⅱ:滴加溶液到10 mL时,得到的溶液为CH3COOH、CH3COONa等浓度等体积混合。即n(CH3COOH)= n(CH3COONa)根据物料守恒可得①c(CH3COOH)+c(CH3COO-)=2c(Na+).由于CH3COOH的电离作用大于CH3COO-的水解作用,所以c(CH3COO-)> c(CH3COOH),c(H+) >c(OH-)。结合电荷守恒可得②c(CH3COO-)+c(OH-)=c(Na+)+c(H+)。将该式整理得c(Na+)= c(CH3COO-)+c(OH-)-c(H+),代入①式可得c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]。正确。
考点:考查溶液中离子浓度大小比较的知识。

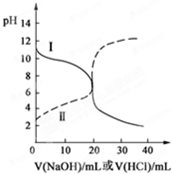 25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1 NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1 NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A、曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | B、曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | C、曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | D、曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |