��Ŀ����
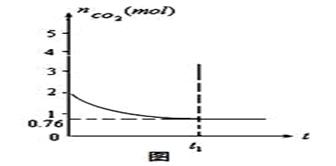
��12�֣�һ���¶���2���ĺ����������У�����2moL̼��2moLCO2�������·�Ӧ�� C(s)+CO2(g)  2CO(g) ��H��0�����������CO2�����ʵ�����ʱ��t�ı仯��ϵ��ͼ��ʾ��
2CO(g) ��H��0�����������CO2�����ʵ�����ʱ��t�ı仯��ϵ��ͼ��ʾ��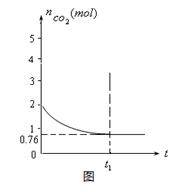
��1���÷�Ӧ�Ħ�S 0������������������������� ����ϸߡ��ϵ͡����¶��������ڸ÷�Ӧ�Է����С�
��2����ʽ�����������¶��´˷�Ӧ��ƽ�ⳣ��K ��
���������һλС����
��3��������ƽ����ϵ����ͨ��CO2����CO2��ת���� ��������С�����䡢��ȷ������
��4����ͬ�¶��£�2���ĺ����������м���4moL̼��4moLCO2���ﵽƽ�⡣����ͼ�л�����������CO2�����ʵ�����ʱ��t�仯��ϵ��Ԥ�ڽ��ʾ��ͼ����ע��ƽ��ʱCO2�����ʵ�����
��5����ͬ�¶��£�2���ĺ����������м���4moL̼��4moLCO2��4moLCO����ʼ��Ӧʱ
V(��) V(��)���������������
��1��> �ϸߣ�2��,��1�֣� ��2��K=c2(CO)/C(CO2)=1.242/0.38="4.0" (3��)
��3�����٣�2�֣� ��4����ͼ��3�֣�����㡢�յ㡢ƽ���߸�1�֣�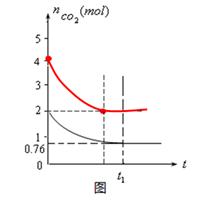 ��5������2�֣�
��5������2�֣�
����

��ϰ��ϵ�д�
�����Ŀ
 2CO(g)
��H��0�����������CO2�����ʵ�����ʱ��t�ı仯��ϵ��ͼ��ʾ��
2CO(g)
��H��0�����������CO2�����ʵ�����ʱ��t�ı仯��ϵ��ͼ��ʾ��