题目内容
7.下列说法不正确的是(NA表示阿伏加德罗常数的值)( )| A. | 28g氮气所含有的原子数目为NA | |
| B. | 常温常压下,32gO2含有的O原子数为NA | |
| C. | 1mol甲烷的质量与NA个甲烷分子的质量之和相等 | |
| D. | 标准状况下,22.4L 甲烷和乙炔的混合气体所含的分子数为NA |
分析 A、氮气由氮原子构成;
B、氧气由氧原子构成;
C、1mol甲烷中含NA个甲烷分子;
D、标况下22.4L任何气体的物质的量为1mol.
解答 解:A、氮气由氮原子构成,故28g氮气中含有的氮原子的物质的量n=$\frac{28g}{14g/mol}$=2mol,个数为2NA个,故A错误;
B、氧气由氧原子构成,故32g氧气中含有的氧原子的物质的量n=$\frac{32g}{16g/mol}$=2mol,个数为2NA个,故B错误;
C、1mol甲烷中含NA个甲烷分子,故1mol甲烷的质量与NA个甲烷分子的质量和相等,故C正确;
D、标况下22.4L任何气体的物质的量为1mol,含有的分子数为NA个,故D正确.
故选AB.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
17.下列气体所含有原子数最多的是( )
| A. | 7.5gC2H6 | B. | 14gN2 | C. | 7gCO | D. | 24gO2 |
18.下列离子方程式书写正确的是( )
| A. | 金属钠加入水中:Na+H2O=Na++OH-+H2↑ | |
| B. | 碳酸氢钙溶液跟氢氧化钠溶液混合:HCO3-+OH-=CO32-+H2O | |
| C. | 氢氧化钡溶液滴入硫酸氢钠溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| D. | 亚硫酸钠和足量的稀硝酸混合:SO32-+2H+=SO2↑+H2O |
2.下列说法正确的是( )
| A. | 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 | |
| B. | 实验室制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 | |
| C. | 单质硅是生产光纤制品的基本原料 | |
| D. | 水玻璃可用于生产黏合剂和防火剂 |
12.现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,酸的电离平衡常数如下:
写出下列反应的离子方程式:
CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
17.下列离子反应方程式正确的是( )
| A. | 澄清石灰水来吸收氯气:Cl2+OH-═Cl-+ClO-+H+ | |
| B. | 将金属Na加入冷水中:Na+2H2O═2Na++2OH-+H2↑ | |
| C. | 向稀硝酸中加入少量铁粉:3Fe+8H++2NO3═3Fe2++2NO↑+4H2O | |
| D. | 碳酸氢钙溶液中加入少量苛性钾溶液:OH-+Ca2++HCO3-=H2O+CaCO3↓ |
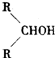 最难
最难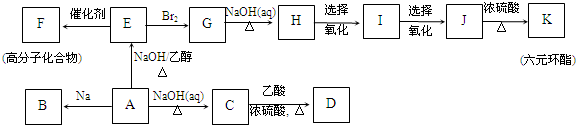
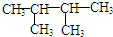 ,K为
,K为 ;
;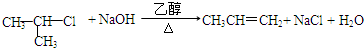 ;G→H
;G→H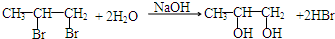 ;
;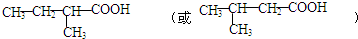 .
.