题目内容
【题目】下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是
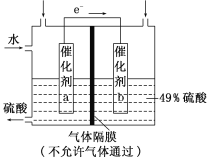
A. 该装置将化学能转化为电能
B. 催化剂b表面O2发生还原反应,其附近酸性增强
C. 催化剂a表面的反应是:SO2+2H2O-2e-===SO42-+4H+
D. 若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8∶15
【答案】B
【解析】
A.该装置没有外加电源,是一个原电池,把化学能转化为电能,故A正确;B.由图示可看出,电子由a表面转移到b表面,因此a表面发生氧化反应,由题意SO2转化为H2SO4发生氧化反应,因此催化剂a表面SO2发生氧化反应,催化剂b表面O2发生还原反应生成H2O,消耗H+,其附近酸性减弱,故B错误;C.催化剂a表面是SO2失去电子生成硫酸,电极方程式为:SO2+2H2O-2e-=SO42-+4H+,故C正确;D.催化剂a处的反应为:SO2+2H2O-2e-=SO42-+4H+,催化剂b处的反应为:![]() O2+2H++2e-=H2O,总方程为:SO2+H2O+
O2+2H++2e-=H2O,总方程为:SO2+H2O+![]() O2=H2SO4,设加入的SO2为xg,H2O为yg。则生成硫酸的质量为:
O2=H2SO4,设加入的SO2为xg,H2O为yg。则生成硫酸的质量为:![]() =
=![]() g,水的质量变化为:y-
g,水的质量变化为:y-![]() =(y-
=(y-![]() )g,根据硫酸浓度仍为49%,则
)g,根据硫酸浓度仍为49%,则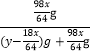 =49%,可以求得
=49%,可以求得![]() =
=![]() ,故D正确;故选B。
,故D正确;故选B。

 名校课堂系列答案
名校课堂系列答案【题目】球形尖晶石(LiMn2O4)属于等轴晶系,可作耐火材料,常用低温电解法制备,制备过程中的能量转化形式是( )
A.电能转化为化学能B.化学能转化为电能
C.机械能转化为化学能D.化学能转化为机械能
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:

相对分子质量 | 密度/(gcm3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |

实验步骤:
在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的名称是:__________________。
(2)在洗涤操作中,第一次水洗的主要目的是:________________;第二次水洗的主要目的是:________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a. 直接将乙酸异戊酯从分液漏斗上口倒出
b. 直接将乙酸异戊酯从分液漏斗下口放出
c. 先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d. 先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:________________________________。
(5)实验中加入少量无水MgSO4的目的是:________________________________。
(6)本实验的产率是:________________(填标号)。
a. 30% b. 40% c. 50% d. 60%
(7)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏______(填“高”或“低”),其原因是________________________________。