题目内容
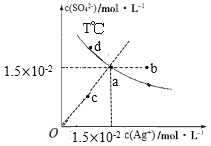
【题目】中成药连花清瘟胶囊中有效成分为绿原酸。已知绿原酸存在如图转化,下列有关说法正确的是
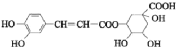 (绿原酸)
(绿原酸)![]()
 (化合物I) +
(化合物I) +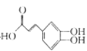 (化合物II)
(化合物II)
A.在反应①中,绿原酸与水按 1∶1 发生反应,则绿原酸的分子式为C16H20O10
B.1 mol化合物Ⅰ与足量金属钠反应生成氢气体积为56L
C.绿原酸、化合物I、化合物II均能发生氧化反应、取代反应、消去反应
D.化合物II中所有碳原子可能都共面
【答案】D
【解析】
A.根据绿原酸的结构简式可知其分子式为C16H18O9,故A错误;
B.未标明温度和压强,无法计算气体体积,故B错误;
C.化合物II中羟基与苯环直接相连,无法发生消去反应,故C错误;
D.苯环上的碳原子共面,碳碳双键上的碳原子及与双键上碳原子相连的碳原子形成一个平面,苯环平面与双键平面以单键相连,单键可以旋转,所以该化合物中所有碳原子可能都共面,故D正确;
故答案为D。

 名校课堂系列答案
名校课堂系列答案【题目】欲降低废水中重金属元素铬的毒性,可将![]() 转化为Cr(OH)3沉淀除去。几种金属离子生成沉淀的pH如下表。
转化为Cr(OH)3沉淀除去。几种金属离子生成沉淀的pH如下表。
阳离子 | Fe3+ | Fe2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | —— | —— |
沉淀完全时的pH | 3.2 | 9.0 | 9(>9溶解) | 8 |
(1)某含铬废水处理的主要流程如下图所示:

①初沉池中加入明矾作沉降剂,其作用的原理是(用离子方程式表示)______________________________。
②请补充并配平以下反应池中发生主要反应的离子方程式:____![]() +____
+____![]() +____===____Cr3++____
+____===____Cr3++____![]() +____H2O。
+____H2O。
③根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是:H++OH-===H2O和_______________________________。证明Cr3+沉淀完全的方法是_____________________________________________________________。
(2)工业可用电解法来处理含![]() 的废水。实验室利用如图模拟处理含
的废水。实验室利用如图模拟处理含![]() 的废水,阳极反应是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。
的废水,阳极反应是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。

①Fe2+与酸性溶液中的![]() 反应的离子方程式是______________________________。
反应的离子方程式是______________________________。
② 若溶液中含有0.01 mol ![]() ,则阳离子全部生成的沉淀的物质的量是______mol。
,则阳离子全部生成的沉淀的物质的量是______mol。