题目内容
【题目】下列对一些实验事实的理论解释正确的是( )
选项 | 实验事实 | 理论解释 |
A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
B | SO2为V形分子 | SO2分子中S原子采用sp3杂化 |
C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
A. AB. BC. CD. D
【答案】A
【解析】
A.原子轨道中电子处于全空、半满、全满时较稳定,氮原子2p能级半充满,则氮原子的第一电离能大于同一周期相邻的氧原子,故A正确;
B.SO2中S的价层电子对数=2+![]() =3,为sp2杂化,立体构型为V形,故B错误;
=3,为sp2杂化,立体构型为V形,故B错误;
C.金刚石为原子晶体,石墨为混合型晶体,但石墨中共价键的键长比金刚石中共价键键长短,键能更大,所以石墨的熔点比金刚石的高,故C错误;
D.卤族元素氢化物都属于分子晶体,分子晶体的沸点随着其相对分子质量的增大而增大,但氟化氢分子间含有氢键,氯化氢中不含氢键,导致氟化氢沸点高于HCl,故D错误;
答案选A。

 期末集结号系列答案
期末集结号系列答案【题目】氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。
Ⅰ. 某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照下表所示的方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液+1 mL H2O | 1 mL 0.1 mol·L-1FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+1 mL HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+1 mL NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(1)实验①和②的目的是___。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是__________(写出一种即可)。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图1所示。分析该图能够得出的实验结论是____。
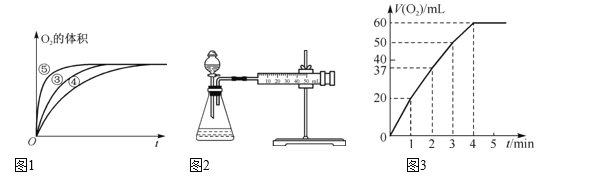
Ⅱ. MnO2对H2O2的分解有催化作用,某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将状态不同的0.1 g MnO2分别加入盛有50 mL等浓度的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2状态 | 触摸试管情况 | 观察结果 | 反应完成所需时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 4 min |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(1)写出大试管中发生反应的化学方程式:__,该反应是____反应(填“放热”或“吸热”)。
(2)实验结果表明,催化剂的催化效果与____有关。
(3)实验过程中放出气体的体积(标准状况)和时间的关系如图3所示。解释反应速率变化的原因:__,计算H2O2的初始物质的量浓度为____。(保留两位有效数字)
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
第二周期 | ① | ② | ③ | |||||
第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
第四周期 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:__(填元素符号),
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子__,碱性最强的化合物的电子式是:__。
(3)用电子式表示元素④与⑥的化合物的形成过程:__。
(4)表示①与⑦的化合物的电子式__,该化合物是由__(填“极性”或“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是_(用化学式表示)。
(6)元素③的简单氢化物的结构式__,在常温下和元素⑦的单质反应的离子方程式__。
【题目】在催化剂作用下,氮氧化物与一氧化碳能发生反应,如:
![]()
![]()
![]() 反应Ⅰ
反应Ⅰ
(1)已知:![]()
![]() 反应Ⅱ
反应Ⅱ
![]()
![]() 反应Ⅲ
反应Ⅲ
①![]() __________(用含b、c的代数式表示)。
__________(用含b、c的代数式表示)。
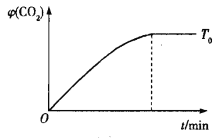
②温度为![]() 时,CO与
时,CO与![]() 在密闭容器中发生反应Ⅲ,
在密闭容器中发生反应Ⅲ,![]() 的体积分数
的体积分数![]() 随时间变化的关系如下图所示。请在坐标图中画出温度为
随时间变化的关系如下图所示。请在坐标图中画出温度为![]() 时,
时,![]() 随时间的变化曲线并进行相应的标注。_______
随时间的变化曲线并进行相应的标注。_______
(2)在恒压条件下,将NO和CO置于密闭容器中发生反应Ⅰ,在不同温度、不同投料比![]() 时,NO的平衡转化率见下表:
时,NO的平衡转化率见下表:
| 300K | 400K | 500K |
1 | 15% | 24% | 33% |
2 | 10% | 18% | 25% |
a__________(填“>”“<”或“=”)0,理由是_________。试判断反应Ⅰ在常温下能否自发进行并说明理由:___。
②下列措施有利于提高CO平衡转化率的是__________(填字母)。
A.升高温度同时增大压强
B.继续通入CO
C.加入高效催化剂
D.及时将![]() 从反应体系中移走
从反应体系中移走
③500 K时,将投料比为2的NO与CO混合气体共0.9 mol,充入一装有催化剂且体积为3 L的密闭容器中,5 min时反应达到平衡,则500 K时该反应的平衡常数K为__________(保留两位小数,下同);从反应开始到达到平衡时CO的平均反应速率为__________![]() 。
。