题目内容
【题目】各城市为保持街道整洁、湿润,在路面或广场上喷洒含化学式为XY2的溶液作保湿剂。X原子的结构示意图为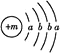 ,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
(1)m=________,该保湿剂的化学式为________。
(2)Z、W元素的名称分别为________、________。
(3)下列说法正确的是________。
A. XY2和WZ2都为离子化合物
B. XY2中仅含离子键,WZ2中仅含极性共价键
C. H2Z比HY的稳定性强
D. X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________。
A. XY2的电子式:![]()
B. WZ2的结构式:Z=W=Z
C. Y元素的单质与H2Z水溶液反应的离子方程式:Y2+Z2-=2Y-+Z↓
【答案】20 CaCl2 硫 碳 B B
【解析】
X原子的结构示意图为 ,由于K层最多容纳2个电子,L层最多容纳8个电子,可知a=2,b=8,核电荷数为20,故X为Ca元素;由化学式XY2可知Y的化合价为-1价,而X的阳离子与Y的阴离子的电子层结构相同,则离子核外电子数相等,Ca2+核外电子数为18,则Y原子核外电子数为17,故Y为Cl元素,则该保湿剂为CaCl2;元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,符合条件的元素有He、C、S,由于Z与Y相邻且Z、W能形成一种WZ2型分子,则Z为S元素,W为C元素,二者形成的分子为CS2,据此解答。
,由于K层最多容纳2个电子,L层最多容纳8个电子,可知a=2,b=8,核电荷数为20,故X为Ca元素;由化学式XY2可知Y的化合价为-1价,而X的阳离子与Y的阴离子的电子层结构相同,则离子核外电子数相等,Ca2+核外电子数为18,则Y原子核外电子数为17,故Y为Cl元素,则该保湿剂为CaCl2;元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,符合条件的元素有He、C、S,由于Z与Y相邻且Z、W能形成一种WZ2型分子,则Z为S元素,W为C元素,二者形成的分子为CS2,据此解答。
(1) 由上述分析可知,m=20,该保湿剂的化学式为CaCl2;
(2) 由上述分析可知,Z、W元素的名称为硫、碳;
(3) A. XY2是CaCl2,为仅含离子键的离子化合物,WZ2是CS2,为仅含极性键的共价化合物,A错误;
B. 由A项分析可知,CaCl2中仅含有离子键,CS2中仅含有极性共价键,B正确;
C. 同周期从左到右,非金属性依次减弱,则S的非金属性弱于Cl,根据非金属性越强,氢化物越稳定,则H2S的稳定性比HCl弱,C错误;
D. Ca2+、Cl-具有相同的电子层结构,电子层相同的粒子,核电荷数越大,半径越小,所以Ca2+的核电荷数大,半径小,D错误。
答案选B;
(4)A. XY2为CaCl2,其电子式为![]() -Ca2+
-Ca2+![]() -,A错误;
-,A错误;
B. WZ2为CS2,结构式为S=C=S,B正确;
C. H2S为弱酸,应写成化学式,即Cl2+H2S=2H++2Cl-+S↓,C错误。
答案选B。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案