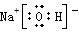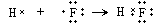题目内容
书写电子式或用电子式回答下列问题①NaOH ②H2O ③O=C=O ④CCl4
⑤以氟化氢为例表示共价键形成过程
⑥以硫化钠为例表示离子键形成过程 .
【答案】分析:首先判断化合物的类型,离子化合物阴离子带电荷且用“[]”,共价化合物不带电荷,注意各原子或离子满足稳定结构.
解答:解:①NaOH为离子化合物,电子式为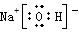 ,故答案为:
,故答案为: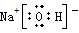 ;
;
②H2O为共价化合物,电子式为 ,故答案为:
,故答案为: ;
;
③O=C=O为共价化合物,C=O之间含有两对电子,满足8电子稳定结构,电子式为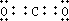 ,
,
故答案为: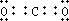 ;
;
④CCl4为共价化合物,各原子满足8电子稳定结构,电子式为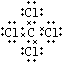 ,故答案为:
,故答案为: ;
;
⑤HF为共价化合物,各原子满足8电子稳定结构,共价键形成过程为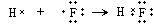 ,
,
故答案为: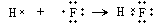 ;
;
⑥硫化钠为离子化合物,离子和原子都满足8电子稳定结构,离子键形成过程为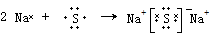 ,
,
故答案为: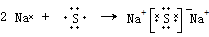 .
.
点评:本题考查电子式的书写,题目难度不大,注意共价化合物和离子化合物的电子式书写方法的不同.
解答:解:①NaOH为离子化合物,电子式为
②H2O为共价化合物,电子式为
③O=C=O为共价化合物,C=O之间含有两对电子,满足8电子稳定结构,电子式为
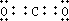 ,
,故答案为:
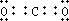 ;
;④CCl4为共价化合物,各原子满足8电子稳定结构,电子式为
⑤HF为共价化合物,各原子满足8电子稳定结构,共价键形成过程为
故答案为:
⑥硫化钠为离子化合物,离子和原子都满足8电子稳定结构,离子键形成过程为
故答案为:
点评:本题考查电子式的书写,题目难度不大,注意共价化合物和离子化合物的电子式书写方法的不同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目