题目内容
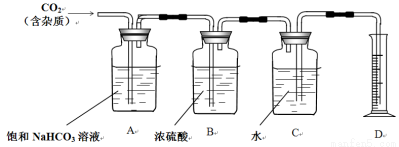
下列方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是 ( )
A.取a克混合物充分加热,残留固体b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量Ba(OH)2溶液充分反应,最终得b克BaCO3
D.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D
【解析】
试题分析:A、NaHCO3受热易分解生成碳酸钠、水和二氧化碳,所以通过加热分解利用差量法即可计算出Na2CO3质量分数,故A不选;B、Na2CO3和NaHCO3均可与盐酸反应生成水、二氧化碳和氯化钠,所以bg固体是氯化钠,利用守恒法可计算出Na2CO3质量分数,故B不选;C、Na2CO3和NaHCO3都与Ba(OH)2反应,反应的方程式为CO32-+Ba2+=BaCO3↓、HCO3-+OH-+Ba2+=H2O+BaCO3↓,因此最后得到的固体是BaCO3,所以可以计算出Na2CO3质量分数,故C不选;D、混合物与足量稀硫酸充分反应,也会生成水和二氧化碳,所以逸出的气体是二氧化碳,但会混有水蒸气,即碱石灰增加的质量不是二氧化碳的质量,不能测定含量,故D选,答案选D。
考点:考查实验方案设计与评价

 阅读快车系列答案
阅读快车系列答案在呼吸面具和潜水艇中可用Na2O2作为供氧剂,请选择适当的化学试剂和实验用品,用下图中的实验装置进行试验,证明Na2O2可作供氧剂。
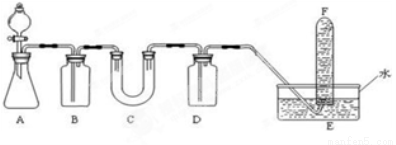
(1)A是制取CO2的装置。在实验室里,CO2常用稀盐酸与石灰石反应来制取,反应的化学方程式为: 。(2分)
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | (2分) |
C | Na2O2 | (2分) |
D | NaOH溶液 | (2分) |
(3)Na2O2与CO2反应的化学方程式: 。(2分)
(4)试管F中收集满气体后,下一步验操作是: 。(2分)