题目内容
Ⅰ.某元素有6个电子处于第三电子层d轨道上,推测该元素的原子序数是________,并根据洪特规则推测在第三电子层d轨道上未成对电子的个数是________个。
Ⅱ.核电荷数小于18的两种元素,A原子最外层电子数为a个,次外层电子数为b个;B原子M层电子数为(a-b)个,L层为(a+b)个,则:
(1)写出元素的名称和符号:A.____________________,B.____________________。
(2)写出各原子的核外电子排布的轨道表示式。
Ⅱ.核电荷数小于18的两种元素,A原子最外层电子数为a个,次外层电子数为b个;B原子M层电子数为(a-b)个,L层为(a+b)个,则:
(1)写出元素的名称和符号:A.____________________,B.____________________。
(2)写出各原子的核外电子排布的轨道表示式。
Ⅰ.26 4
Ⅱ.(1)氧元素、O 硅元素、Si
(2)O: Si:
Si: 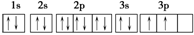
Ⅱ.(1)氧元素、O 硅元素、Si
(2)O:
 Si:
Si: 
Ⅰ.由于3d轨道上有6个电子,说明该元素原子的电子排布式为1s22s22p63s23p63d64s2,即为Fe元素,根据洪特规则“电子尽量分布在不同的轨道上且ms相同”,判断3d上有4个未成对电子。Ⅱ.根据B原子L层电子数为(a+b)个,判断a+b=8,说明b<8,那么A原子次外层电子数为b个,b只能为2,那么a=6,推测A为O,B为Si。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目