题目内容
7.下列现象与氢键有关的是( )①NH3的熔、沸点比第ⅤA族其他元素氢化物的熔、沸点高
②碳原子数较少的醇、羧酸可以和水以任意比互溶
③常温下H2O为液态,而H2S为气态
④水分子高温下也很稳定.
| A. | .①②③④ | B. | .①②③ | C. | ②③④ | D. | .① |
分析 ①ⅤA族中,N的非金属性最强,NH3中分子之间存在氢键;
②醇、羧酸与水分子之间能形成氢键;
③水分子与分子间存在氢键,所以常温下H2O为液态,而H2S分子间无氢键,所以常温下为气态;
④稳定性与化学键有关.
解答 解:①因第ⅤA族中,N的非金属性最强,NH3中分子之间存在氢键,则NH3的熔、沸点比VA族其他元素氢化物的高,故①正确;
②小分子的醇、羧酸与水分子之间能形成氢键,则可以和水以任意比互溶,故②正确;
③水分子与分子间存在氢键,所以常温下H2O为液态,而H2S分子间无氢键,所以常温下为气态,故③正确;
④水分子高温下也很稳定,其稳定性与化学键有关,而与氢键无关,故④错误;
故选B.
点评 本题考查氢键及氢键对物质的性质的影响,明确氢键主要影响物质的物理性质是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
17.某种药物合成中间体的结构简式为: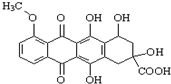 ,有关该物质的说法不正确的是( )
,有关该物质的说法不正确的是( )
 ,有关该物质的说法不正确的是( )
,有关该物质的说法不正确的是( )| A. | 该化合物属于芳香族化合物,分子式为C20H16O9 | |
| B. | 能发生消去反应、酯化反应、取代反应、氧化反应、水解反应等 | |
| C. | 能分别与金属Na、NaHCO3溶液反应 | |
| D. | 1 mol该有机物与足量NaOH溶液反应,消耗3 mol NaOH |
15.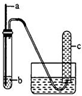 按如图所示装置选取不同试剂组进行实验,下列实验现象预期和结论均正确的是
按如图所示装置选取不同试剂组进行实验,下列实验现象预期和结论均正确的是
( )
 按如图所示装置选取不同试剂组进行实验,下列实验现象预期和结论均正确的是
按如图所示装置选取不同试剂组进行实验,下列实验现象预期和结论均正确的是| a | b | 实验现象预期 | 结论 | |
| A | 铜丝 | 浓硝酸 | 试管c中有大量红棕色气体 | 硝酸有强氧化性 |
| B | 木条 | 18.4mol/L硫酸 | 木条变黑 | 浓硫酸有酸性及氧化性 |
| C | 生铁 | 饱和NaCl溶液 | 导管中发生倒吸 | 生铁发生吸氧腐蚀 |
| D | 铁丝 | 含少量HCl的H2O2溶液 | 试管c中有大量无色气体 | 该反应中铁做催化剂 |
| A. | A | B. | B | C. | C | D. | D |
2.乙炔分子中有3个σ键、两个π键,它们分别是( )
| A. | C-H之间是sp形成的σ键,C-C之间全是未参加杂化的2p轨道形成的π键 | |
| B. | C-C之间是sp形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键 | |
| C. | sp杂化轨道形成σ键、未杂化的两个2p轨道形成两个π键,且杂化轨道与未杂化轨道互相平行 | |
| D. | sp杂化轨道形成σ键、未杂化的两个2p轨道形成两个π键,且杂化轨道与未杂化轨道互相垂直 |
12.向蔗糖晶体中加入一定量的浓硫酸,发现蔗糖晶体变黑、膨胀,此过程中浓硫酸没有表现的性质是( )
| A. | 脱水性 | B. | 强氧化性 | C. | 酸性 | D. | 吸水性 |
16.有某硫酸和硝酸的混合溶液20mL,其中含有硫酸的浓度为2mol•L-1,含硝酸的浓度为1mol•L-1,现向其中加入3.2g铜粉,充分反应后(假设只生成NO气体),最多可收集到标况下的气体的体积为( )
| A. | 89.6mL | B. | 112mL | C. | 224 mL | D. | 448mL |
6.有机化合物M是中药狼把草的成分之一,它具有消炎杀菌作用,M的结构如图所示,下列叙述正确的是( )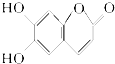

| A. | M的摩尔质量是180g/mol | |
| B. | 1 mol M最多能与2 mol Br2发生反应 | |
| C. | 1 mol M与足量NaHCO3反应能生成4 mol CO2 | |
| D. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 |