题目内容
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(1)该反应的离子方程式为 。
(2)用“双线桥”表示出反应中电子转移的方向和数目:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(3)氧化产物与还原产物的质量之比为 。
(4)如果反应中转移0.2mol电子,则生成I2的物质的量为_________mol。
【答案】
(1)IO3-+5I -+6H+=3I2+3H2O
(2)
(3)5:1
(4)0.12
【解析】
试题分析:(1)根据反应的化学方程式可知该反应的离子方程式为IO3-+5I -+6H+=3I2+3H2O。
(2)碘酸钾中碘元素的化合价从+5价降低到0价,得到5个电子,碘化钾中碘元素的化合价从-1价升高到0价,因此用“双线桥”表示出反应中电子转移的方向和数目为
 。
。
(3)还原剂与氧化剂的物质的量之比是5:1,则氧化产物与还原产物的质量之比为5:1。
(4)生成3mol碘转移5mol电子,如果反应中转移0.2mol电子,则生成I2的物质的量为
![]() 。
。

练习册系列答案
相关题目
【题目】Ⅰ、有机物分子中的一个碳原子所连的4个原子或原子团均不相同时,该碳原子称为手性碳原子,含有手性碳原子的化合物具有光学活性,某有机物X(结构如下)具有光学活性(式中标有*号的碳为手性碳原子),欲使其保持光学活性,发生以下 (选填序号)反应,该有机物仍一定具有光学活性。
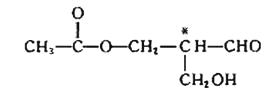
A.消去反应 | B.水解反应 | C.银镜反应 | D.酯化反应 |
Ⅱ、写出由1-溴丁烷和必要的无机试剂制取1,2-二溴丁烷的化学方程式