题目内容
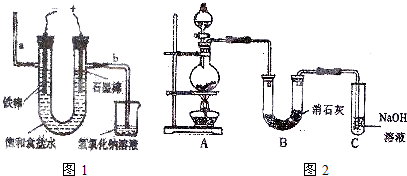
在加热条件下,浓H2SO4可与食盐制取浓HCl、浓HCl可与KMnO4制取Cl2,选用下图所示装置(含有所盛放的试剂)设计实验。

(1)写出上述制取浓HCl,Cl2的化学反应方程式:
______________________________________________________;
______________________________________________________。
(2)用仪器间相互连接处的数字,表示四种仪器之间的连接顺序:
______________________________________。
(3)上图C中的饱和食盐水的作用是 ;
B中的氢氧化钠溶液的作用是 。
(4)反应装置D中有一处连接错误是 ;
实验装置中有Cl2生成的现象是 ;
(5)写出氯气与氢氧化钠溶液反应的化学方程式
⑴ H2SO4(浓) + 2NaCl ![]() Na2SO4 + 2HCl↑
Na2SO4 + 2HCl↑
16HCl + 2KMnO4 = 2 KCl + 2MnCl2 + 8H2O + 5Cl2↑
⑵ 1 5 6 3 4 2
⑶ 吸收逸出的氯化氢 吸收氯气
⑷ 5(6)处应为长进短出 黄绿色气体充满C或D装置
⑸ Cl2 + 2OH- = Cl- + ClO- + H2O

练习册系列答案
相关题目