题目内容
将相同质量的镁条分别在①氧气;②空气;③氮气;④二氧化碳中完全燃烧,燃烧后所得固体产物的质量由小到大的顺序是( )A.②<①<③<④ B.④=①=②=③ C.③<②<①<④ D.③<①<②<④
解析:首先写出镁条在各气体中燃烧的化学方程式:
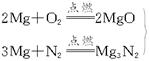 (空气中的主要反应)
(空气中的主要反应)
2Mg+CO2![]() 2MgO+C(CO2中的反应)
2MgO+C(CO2中的反应)
设有1 mol Mg完全反应:
①1 mol Mg在O2中燃烧得1 mol MgO,质量增加16 g;②由于Mg在空气中燃烧的产物既有MgO,又有Mg3N2,故1 mol Mg在空气中燃烧固体质量增加在9.3—![]() =9.3 g;④1 mol Mg在CO2中燃烧得1 mol MgO和
=9.3 g;④1 mol Mg在CO2中燃烧得1 mol MgO和![]() mol C,质量增加
mol C,质量增加![]() =
=
答案:C

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知镁能在O2里燃烧,也能在CO2里燃烧(反应方程式为2Mg+CO2═2MgO+C),还能在N2里燃烧(3Mg+N2═Mg3N2).将相同质量的镁条分别在①氧气中;②空气中;③氮气中;④二氧化碳中完全燃烧,燃烧后所得固体产物的质量由小到大的顺序( )
| A、③<②<①=④ | B、④=①=②=③ | C、③<②<①<④ | D、③<①<②<④ |