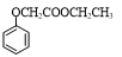题目内容
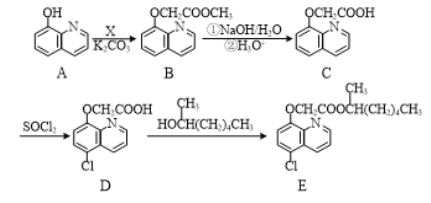
【题目】有机物E是一种药物中间体,合成路线如下:

(1)该路线中设计第Ⅰ、Ⅲ步的目的是________。
(2)步骤Ⅳ中X的结构简式为________。
(3)1 mol E与足量的H2反应,最多消耗H2_________mol。
(4)F是C的一种同分异构体,能与新制的氢氧化铜反应生成红色沉淀,遇FeCl3溶液显紫色,分子中含有4种不同环境的氢。F的结构简式为_________。
【答案】保护酚羟基(防止被氧化) 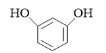 7
7 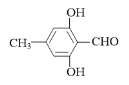 或
或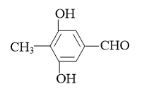
【解析】
A在K2CO3作用下和CH3I发生取代反应生成B,B中的甲基被高锰酸钾溶液氧化生成C,C在与HI发生反应生成D ,D与C6H6O2发生取代反应生成E,结合E的结构简式,可知X的结构简式为 ,据此分析解答。
,据此分析解答。
(1)该路线中设计第Ⅰ将酚羟基转化为醚键,第Ⅲ步将醚键转化为酚羟基,由于第Ⅱ步中使用高锰酸钾溶液氧化甲基,第Ⅰ、Ⅲ步目的是保护酚羟基(防止被氧化);
(2)根据分析,结合E和D的结构简式可知,步骤Ⅳ中X的结构简式为 ;
;
(3)E中含有羰基和苯环,都能与氢气发生加成反应,则1 mol E与足量的H2反应,最多消耗7mol H2;
(4)F是C的一种同分异构体,能与新制的氢氧化铜反应生成红色沉淀,说明结构中含有醛基,遇FeCl3溶液显紫色,说明结构中含有酚羟基和苯环,分子中含有4种不同环境的氢,结合C的结构简式,F的结构简式为 或
或 。
。

【题目】下列根据实验操作和实验现象所得出的结论,正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向亚硫酸钠试样中滴入盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 试样已经氧化变质 |
B | 乙醇和浓硫酸混合加热至170℃,将产生气体通入酸性KMnO4溶液 | 紫红色褪去 | 使溶液褪色的是乙烯 |
C | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
D | 将炽热的木炭与浓硝酸混合所得气体通入澄清石灰水中 | 澄清石灰水不变浑浊 | 验证碳的氧化产物为CO |
A.AB.BC.CD.D