题目内容
按要求回答问题
(1)NaHSO4与NaHCO3溶液反应 。
(2)KClO3+6HCl=KCl+3Cl2↑+3H2O氧化剂与还原剂的物质的量的比为 。氧化产物与还原产物的物质的量的比 。
(3)已知下面三个反应:2Fe2++Cl2=2Fe3++2Cl- ;2Fe2++Br2=2Fe3++2Br-; 2Br-+Cl2=Br2+2Cl-
①根据以上三个反应,判断还原剂的还原性由强到弱的顺序 。
②写出氯气和溴化亚铁以物质的量之比为3:4的离子反应方程式 。
温度为T时,在4.0 L恒容密闭容器中充入2.0 mol PCl5,发生反应:
PCl5(g) PCl3(g)+Cl2(g),反应时间(t)与容器内气体总压强(p)的数据见下表:
PCl3(g)+Cl2(g),反应时间(t)与容器内气体总压强(p)的数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
总压强p/100kPa | 100 | 116 | 119 | 120 | 120 |
(1)由总压强p和起始压强p0计算反应物PCl5的转化率α(PCl5)的表达式为?平衡时PCl5的转化率为多少?
(2)反应在前50 s的平均速率v(PCl3)为多少?
(3)该温度下 的平衡常数为多少?
的平衡常数为多少?
A.在500 mL容量瓶中配制500 mL烧碱溶液 |
B.用移液管(或碱式滴定管)量取50.00 mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂 |
C.在天平上准确称取烧碱样品m g,在烧杯中加蒸馏水溶解 |
D.将物质的量浓度为c mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1mL |
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2mL 请完成下列问题:
(1)正确的操作步骤是(填写字母)________→________→________→D→________.
(2)滴定管读数应注意_______________________.
(3)操作中锥形瓶下垫一张白纸的作用是___________________.
(4)操作D中液面应调整到________________________;尖嘴部分应____________.
(5)滴定到终点时锥形瓶内溶液的pH约为___________;终点时的颜色变化是________.
(6)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响________(填“偏高”、“偏低”或“无影响”,其他操作均正确).
(7)该烧碱样品的纯度计算式是__________________.


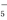 与Fe2+之间形成的化学键类型是离子键
与Fe2+之间形成的化学键类型是离子键 ,则其中仅有1个碳原子采取sp3杂化
,则其中仅有1个碳原子采取sp3杂化 CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施能提高COCl2转化率的是 2AlN+3CO。有关该反应下列叙述正确的是( )
2AlN+3CO。有关该反应下列叙述正确的是( ) B.
B. m=
m=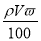 C.ρ=
C.ρ=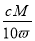 D.w%=
D.w%=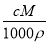 %
% 、OH-等3
、OH-等3