题目内容
氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3.请回答下列问题:
(1)NH3的电子式是
 .
.
(2)Na3N与盐酸反应生成
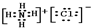

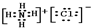 .
.
(1)NH3的电子式是


(2)Na3N与盐酸反应生成
2
2
种盐,其电子式是
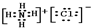

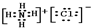
分析:(1)根据共价化合物电子式的书写规则书写;
(2)先写出氮化钠和水反应的方程式,再写出氨气和氢氧化钠与盐酸反应的方程式,根据方程式判断生成盐的种类,并写出电子式.
(2)先写出氮化钠和水反应的方程式,再写出氨气和氢氧化钠与盐酸反应的方程式,根据方程式判断生成盐的种类,并写出电子式.
解答:解:(1)A氨气是共价化合物,各原子间通过共用电子对形成共价键,所以其电子式为: .
.
故答案为: .
.
(2分) Na3N+3H2O=NH3+3NaOH ①
NH3+HCl=NH4Cl ②
NaOH+HCl=NaCl+H2O ③
所以生成的盐有2种,分别是 NH4Cl、NaCl.
NH4Cl 和NaCl都是离子化合物,所以其电子式分别为 、
、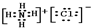 .
.
故答案为:2; 、
、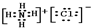 .
.
 .
.故答案为:
 .
.(2分) Na3N+3H2O=NH3+3NaOH ①
NH3+HCl=NH4Cl ②
NaOH+HCl=NaCl+H2O ③
所以生成的盐有2种,分别是 NH4Cl、NaCl.
NH4Cl 和NaCl都是离子化合物,所以其电子式分别为
 、
、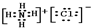 .
.故答案为:2;
 、
、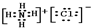 .
.点评:本题考查了电子式的书写,先写出氮化钠与水反应的方程式,再根据酸碱中和反应判断最后生成物,能正确判断氮化钠与盐酸反应的生成物是解本题的关键,

练习册系列答案
相关题目

 、
、