题目内容
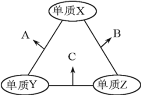
【题目】有X、Y、Z三种短周期元素,原子半径由大到小的顺序为Y>X>Z,原子序数之和为16。三种元素的常见单质在适当条件下可发生如图所示的变化,其中B和C均为10电子分子,以下说法不正确的是
A.A和C不可能发生氧化还原反应
B.X元素位于ⅥA族
C.A不能溶解于B中
D.B的沸点高于C的沸点
【答案】A
【解析】
B和C均为10电子分子,考虑为氢化物,由原子半径由大到小的顺序为Y>X>Z可知,Z为氢,X、Y、Z原子序数之和为16,则X、Y的原子序数之和为15,则Y为碳元素、X为氟元素或者Y为氮元素、X为氧元素,由转化关系,单质X、Y反应生成A,单质Y、Z生成B,则Y应为氮元素、X应为氧元素,则A为NO、B为H2O、C为NH3,验证符合转化关系。
A.从N元素的化合价分析可知,NO和NH3可能发生归中反应,故能发生氧化还原反应![]() ,故A错误;
,故A错误;
B.氧元素位于第二周期ⅥA族,故B正确;
C.NO不能溶解于H2O,故NO可以用排水法收集,故C正确;
D.由于H2O的分子量比NH3的大,且水分子之间形成两个分子间氢键,而液氨中只能形成一个分子间氢键,故H2O沸点高于NH3的沸点,故D正确;
本题答案为:A

练习册系列答案
相关题目