题目内容
下列说法中不正确的是( )
| A、能使澄清的石灰水变浑浊的气体可能是SO2 |
| B、能使品红溶液褪色将其煮沸溶液又变红的无色气体一定是SO2 |
| C、某强酸性溶液经分析其中含有大量的S2-,SO32- |
| D、用NaHSO3,Na2SO3与浓硫酸反应都可产生SO2 |
考点:二氧化硫的化学性质
专题:氧族元素
分析:A.二氧化硫、二氧化碳均能使澄清的石灰水变浑浊;
B.二氧化硫的漂白性为暂时性的;
C.酸性溶液中S2-、SO32-发生氧化还原反应;
D.NaHSO3、Na2SO3与浓硫酸均可发生强酸制取弱酸的反应.
B.二氧化硫的漂白性为暂时性的;
C.酸性溶液中S2-、SO32-发生氧化还原反应;
D.NaHSO3、Na2SO3与浓硫酸均可发生强酸制取弱酸的反应.
解答:
解:A.二氧化硫、二氧化碳均能使澄清的石灰水变浑浊,则能使澄清的石灰水变浑浊的气体可能是SO2,故A正确;
B.二氧化硫的漂白性为暂时性的,则能使品红溶液褪色将其煮沸溶液又变红的无色气体一定是SO2,故B正确;
C.酸性溶液中S2-、SO32-发生氧化还原反应,则强酸性溶液不可能含有大量的S2-、SO32-,故C错误;
D.NaHSO3、Na2SO3与浓硫酸均可发生强酸制取弱酸的反应,则均可产生SO2,故D正确;
故选C.
B.二氧化硫的漂白性为暂时性的,则能使品红溶液褪色将其煮沸溶液又变红的无色气体一定是SO2,故B正确;
C.酸性溶液中S2-、SO32-发生氧化还原反应,则强酸性溶液不可能含有大量的S2-、SO32-,故C错误;
D.NaHSO3、Na2SO3与浓硫酸均可发生强酸制取弱酸的反应,则均可产生SO2,故D正确;
故选C.
点评:本题考查二氧化硫的性质,为高频考点,把握二氧化硫的制取、漂白性、酸性氧化物的性质为解答的关键,注意选项C中氧化还原反应为易错点,题目难度不大.

练习册系列答案
相关题目
下列关于铯及其化合物的说法中,不正确的( )
| A、氢氧化铯是一种强碱,易溶于水 |
| B、铯与水或酸剧烈反应,都能生成氢气 |
| C、碳酸铯用酒精灯加热可以生成氧化铯和CO2 |
| D、硫酸铯、碳酸铯、硝酸铯都易溶于水 |
25℃、101kPa 下:
①2Na(s)+
O2(g)═Na2O(s)△H1=-414KJ/mol
②2Na(s)+O2(g)═Na2O2(s)△H2=-511KJ/mol
下列说法正确的是( )
①2Na(s)+
| 1 |
| 2 |
②2Na(s)+O2(g)═Na2O2(s)△H2=-511KJ/mol
下列说法正确的是( )
| A、①和②产物的阴阳离子个数比相等 |
| B、①和②生成等物质的量的产物,转移电子数不同 |
| C、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D、0℃、101kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=-317kJ/mol |
下列过程中能引入卤素原子的是( )
| A、在空气中燃烧 | B、取代反应 |
| C、加成反应 | D、加聚反应 |
门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确.根据元素周期律,下列有关X的性质的描述中正确的是( )
| A、X单质易与水反应 |
| B、X形成的氧化物易与水反应生成酸 |
| C、X易形成氧化物XO |
| D、XH4的稳定性比SiH4的低 |
下列有关实验说法不正确的是( )
| A、在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性 |
| B、向少量的火柴头浸泡液中滴加AgNO3、稀HNO3和NaNO2,检验火柴头中的氯元素 |
| C、在2mL紫色的CoCl2溶液中加入浓盐酸,可使溶液显蓝色 |
| D、制备摩尔盐时,最后在蒸发皿中蒸发浓缩溶液,加热至液体表面出现晶膜为止,不能将溶液全部蒸干 |
在密闭容器中一定量混合气体发生反应:x A(g)+y B(g)?z C(g),平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积压缩到原来的
,再达平衡时测得A的浓度为0.8mol/L,下列判断正确的是( )
| 1 |
| 2 |
| A、x+y<z |
| B、平衡向正反应方向移动 |
| C、B的物质的量增大 |
| D、C的体积分数保持不变 |
某高聚物的结构片段如下:
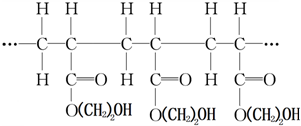
下列分析正确的是( )

下列分析正确的是( )
| A、它是缩聚反应的产物 |
| B、其单体是CH2=CH2COOH和HOCH2CH2OH |
| C、其链节是CH3CH2COO(CH2)2OH |
| D、其单体是CH2=CHCOO(CH2)2OH |