题目内容
【题目】测定放置已久的小苏打样品中纯碱的质量分数.
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算.实验中加热至恒重的目的是 .
(2)方案二:按如图装置进行实验.并回答以下问题: 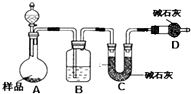
①分液漏斗中应该装(填“盐酸”或“稀硫酸盐”),D装置的作用是 .
②实验中除称量样品质量外,还需称装置反应前后质量的变化(用装置的字母代号);
③根据此实验得到的数据,测定结果有较大误差,因为实验装置还存在一个明显缺陷,该缺陷是 .
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
①实验中判断沉淀已完全的方法是 .
②若加入试剂改为氢氧化钡,已知称得样品9.5g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为 .
【答案】
(1)保证NaHCO3全部分解
(2)稀硫酸;吸收空气中的水蒸气、二氧化碳,防止进入C被吸收;C;装置A、B中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差
(3)在反应后小烧杯的上层清液中,再滴加BaCl2溶液少许,如无白色沉淀出现,说明沉淀完全;56%
【解析】解:(1)该方案根据加热后残渣的质量来求解,要加热至恒重,以保证NaHCO3全部分解.
所以答案是:保证NaHCO3全部分解.(2)①盐酸具有挥发性,会影响实验结果,所以选择稀硫酸;D干燥管中的碱石灰吸收空气中的水蒸气、二氧化碳,防止进入C被吸收,减少误差.
所以答案是:稀硫酸;吸收空气中的水蒸气、二氧化碳,防止进入C被吸收.
②根据所产生的CO2的质量及样品质量,分别求得样品中Na2CO3和NaHCO3的质量从而得出纯碱的质量分数,所以需称量C装置前后质量变化判断生成二氧化碳的质量.
所以答案是:C.
③装置A、B中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差.
所以答案是:装置A、B中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差.(3)①试验中判断沉淀是否完全的方法是:取少量滤液,再滴加BaCl2溶液少许,如无白色沉淀出现,说明沉淀完全.
所以答案是:取少量滤液,再滴加BaCl2溶液少许,如无白色沉淀出现,说明沉淀完全.
②发生反应Na2CO3+Ba(OH)2=BaCO3↓+2NaOH,NaHCO3+Ba(OH)2=BaCO3↓+NaOH+H2O.
样品9.5g,干燥的沉淀碳酸钡质量为19.7g,物质的量为 ![]() =0.1mol,令样品中碳酸钠的物质的量为xmol、碳酸氢钠的物质的量为ymol,
=0.1mol,令样品中碳酸钠的物质的量为xmol、碳酸氢钠的物质的量为ymol,
则106x+84y=9.5,
x+y=0.1,
解得x=0.05,y=0.05,
所以碳酸钠的质量为106g/mol×0.05mol=5.3g,
所以碳酸钠质量分数为 ![]() ×100%=56%.
×100%=56%.
所以答案是:56%.

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案【题目】石油气“芳构化”是由石油气生产高辛烷值汽油的一种有效生产工艺。测得反应2C4H10![]() C8H10(g)+5H2在不同温度下的平衡常数变化如下:
C8H10(g)+5H2在不同温度下的平衡常数变化如下:
温度(℃) | 400 | 450 | 500 |
平衡常数K | a | 6a | 40a |
(1)该反应的正反应是________(填“吸热”或“放热”)反应。
(2)向2 L密闭定容容器中充入2 mol C4H10,反应10 s后测得H2浓度为1 mol·L-1,此10 s内,以C8H10表示的平均速率为____________________。
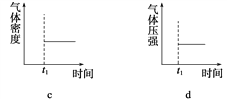
(3)能表示该反应在恒温恒容密闭容器中t1时刻后已经达平衡状态的图示是__________。

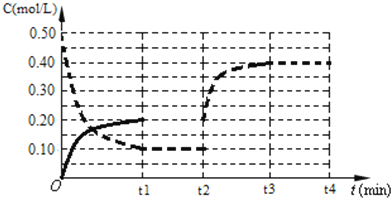
(4)下图表示某温度时将一定量的C4H10(含少量H2)充入容器中反应期间物质浓度随时间的变化(容器容积可变),实线代表C8H10,虚线代表C4H10。请用实线补充画出t1~t4间C8H10的浓度变化曲线。_____________