题目内容
用NA表示阿伏加德罗常数的值,下列说法中正确的是
- A.1molNa2O2中阴阳离子的总数目为4NA
- B.标准状况下,22.4LCCl4含有的共价键数为4NA
- C.标准状况下,14gN2含有的核外电子数为5NA
- D.3mol铁与足量的水蒸气充分反应,转移8NA个电子
D
分析:A、依据过氧化钠的构成离子分析判断;
B、依据气体摩尔体积的条件应用分析;
C、质量换算物质的量结合分子式计算电子数;
D、依据铁和水蒸气反应的电子转移计算判断;
解答:A、1molNa2O2中阴阳离子的总数目为2molNa+和1molO22-,共3mol,故A错误;
B、在标准状况下CCl4不是气体,22.4LCCl4物质的量不是1mol,故B错误;
C、14gN2物质的量=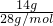 =0.5mol,含有的核外电子数=0.5mol×7×2=7mol,故C错误;
=0.5mol,含有的核外电子数=0.5mol×7×2=7mol,故C错误;
D、铁和水蒸气反应的化学方程式为:3Fe+4H2O Fe3O4+4H2;铁化合价从0价变化为+
Fe3O4+4H2;铁化合价从0价变化为+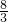 价,3Fe~Fe3O4~8e-,故反应中电子转移为8NA个电子,故D正确;
价,3Fe~Fe3O4~8e-,故反应中电子转移为8NA个电子,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,过氧化钠的离子构成,氧化还原反应的电子转移计算,质量换算物质的量计算电子数,关键是过氧化钠的构成离子.
分析:A、依据过氧化钠的构成离子分析判断;
B、依据气体摩尔体积的条件应用分析;
C、质量换算物质的量结合分子式计算电子数;
D、依据铁和水蒸气反应的电子转移计算判断;
解答:A、1molNa2O2中阴阳离子的总数目为2molNa+和1molO22-,共3mol,故A错误;
B、在标准状况下CCl4不是气体,22.4LCCl4物质的量不是1mol,故B错误;
C、14gN2物质的量=
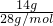 =0.5mol,含有的核外电子数=0.5mol×7×2=7mol,故C错误;
=0.5mol,含有的核外电子数=0.5mol×7×2=7mol,故C错误;D、铁和水蒸气反应的化学方程式为:3Fe+4H2O
 Fe3O4+4H2;铁化合价从0价变化为+
Fe3O4+4H2;铁化合价从0价变化为+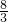 价,3Fe~Fe3O4~8e-,故反应中电子转移为8NA个电子,故D正确;
价,3Fe~Fe3O4~8e-,故反应中电子转移为8NA个电子,故D正确;故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,过氧化钠的离子构成,氧化还原反应的电子转移计算,质量换算物质的量计算电子数,关键是过氧化钠的构成离子.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目