题目内容
19.如图是苯和溴的取代反应的实验装置图,其中A为具有支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量的铁屑粉: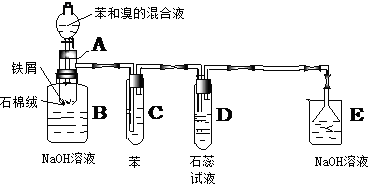
(1)向反应容器A中逐滴加入溴和苯的混合液,写出A中发生反应的化学方程式:2Fe+3Br2=2FeBr3;

(2)试管C中苯的作用是除去溴,反应开始后,D中看到的现象是D管中石蕊试液变红,液面上有白雾
(3)反应2min~3min后,在B中的氢氧化钠溶液里可观察到的现象是溶液中有红褐色的絮状物生成,底部有无色油状物质生成,液面上有白雾
(4)在上述整套装置中,具有防倒吸作用的仪器有DE(填字母).
(5)改进后的实验除:①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这三个优点外,还有一个优点是:环保,不会污染环境.
分析 (1)Fe与溴反应生成溴化铁,苯和液溴在溴化铁作催化剂条件下能发生取代反应生成溴苯与HBr;
(2)溴苯中的溴易挥发,非极性分子的溶质易溶于非极性分子的溶剂;该反应中有溴化氢生成,能与水蒸气结合成氢溴酸液滴,溴化氢溶于水得到氢溴酸,氢溴酸能使石蕊试液变红色;
(3)溴化铁与氢氧化钠反应生成氢氧化铁沉淀,氢氧化钠除去为反应的溴,溴苯与氢氧化钠溶液不互溶;
(4)HBr易溶于水,直接将导管伸入水溶液液面以下,会发生倒吸;
(5)本实验中进行尾气处理,防止污染空气.
解答 解:(1)Fe与溴反应生成溴化铁,苯和液溴在溴化铁作催化剂条件下能发生取代反应生成溴苯与HBr,反应方程式为:2Fe+3Br2=2FeBr3, ,
,
故答案为:2Fe+3Br2=2FeBr3; ;
;
(2)溴苯中的溴易挥发,溴和苯都是非极性分子,根据相似相溶原理知,溴易溶于苯,所以苯的作用是吸收溴蒸汽除去;该反应中有溴化氢生成,能与水蒸气结合成氢溴酸液滴,液面上有白雾,溴化氢溶于水得到氢溴酸,氢溴酸是酸性物质,能使石蕊试液变红色,
故答案为:吸收Br2蒸汽;,D管中石蕊试液变红,液面上有白雾;
(3)苯与液溴发生取代反应生成溴苯和溴化氢,溴苯是密度大于水,无色的油状液体,溴化氢易挥发,能与水蒸气结合成氢溴酸液滴,溴化铁与氢氧化钠反应生成红褐色的氢氧化铁沉淀,
故答案为:溶液中有红褐色的絮状物生成,底部有无色油状物质生成,液面上有白雾;
(4)HBr易溶于水,直接将导管伸入水溶液液面以下,会发生倒吸,装置D中导管口在液面上方,能防止倒吸,E中倒置漏斗增大了气体与氢氧化钠溶液的接触面积,有缓冲作用,能够防止倒吸,
故答案为:DE;
(5)本实验中进行尾气处理,环保,不会污染环境,
故答案为:环保,不会污染环境.
点评 本题为实验制备题目,涉及溴苯的制取,侧重考查学生对装置与原理的分析评价,难度不大.

 小题狂做系列答案
小题狂做系列答案| A. | 溴水 | B. | 碳酸钠溶液 | C. | 紫色石蕊试液 | D. | 金属钠 |
 某研究性学习小组对Cu与H2SO4反应的产物种类和性质进行探究.
某研究性学习小组对Cu与H2SO4反应的产物种类和性质进行探究.Ⅰ.产物种类探究
在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料.
资料1:X射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为中的一种或两种.
资料2:
硫酸/mol•L-1 | 黑色物质出现的温度/°C | 黑色物质消失的温度/°C |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
a.铜与浓硫酸反应时所涉及的反应可能不止一个
b.硫酸浓度选择适当,可避免最后产物中出现黑色物质
c.该反应发生的条件之一是硫酸浓度>15mol•L-1
d.硫酸浓度越大,黑色物质出现越快,越难消失
(2)Cu与足量16mol•L-1浓硫酸反应时,在80°C以后,随着温度的逐渐升高,反应中硫酸铜的生成逐渐增加,而CuS却逐渐减少,到达250°C左右时,CuS在反应中完全消失的澄清溶液,CuS消失的化学方程式为CuS+4H2SO4=CuSO4+4SO2↑+4H2O.
Ⅱ.产物性质探究
Cu与浓H2SO4反应生成的CuSO4具有某些特定性质,一定浓度CuSO4溶液与NaHCO3溶液反应后生成蓝绿色颗粒状沉淀,沉淀可能是CuCO3,Cu(OH)2,或者CuCO3与Cu(OH)2的混合物.
(1)若沉淀是Cu(OH)2,生成沉淀的离子方程式是Cu2++2HCO3-=Cu (OH)2↓+2CO2↑.
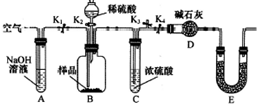
(2)为了进一步探究沉淀的成分,设计的实验装置如图:
实验操作步骤为
a.取沉淀样品100克于B中,检查装置的气密性
b.打开K1,K3,关闭K2,K4,通入足量空气
c.关闭K1,K3,打开K2,K4,充分反应
d.反应结束后,关闭K2,打开K1,再通入足量空气
e.测得装置D的质量增加了22g
①步骤b的作用是排尽装置中空气中的CO2使测定结果准确
②若沉淀样品为CuCO3和Cu(OH)2的混合物,则Cu(OH)2的质量分数为38%,若不进行步骤d,则会使测得Cu(OH)2的质量分数为偏低(填“偏高”“无影响”“偏低”)
| A. | CH2=CH2 | B. | CH3CH=CH2 | C. | CH3CH3 | D. | CH3CH2CH=CH2 |
| A. | 在Na2CO3溶液中:c(OH-)-c(H+)═c(HCO3-)+c(H2CO3) | |
| B. | 在pH=8的NaB溶液中:c(Na+)-c(B-)=9.9×10-7 mol/L | |
| C. | 浓度均为0.1 mol/L的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)═c(HCO3-)+c(H2CO3) | |
| D. | 向10mL pH=12的NaOH溶液中滴加pH=2的HA溶液达中性:则混合液体积V总≥20mL |
C(石墨)+O2(g)═CO2(g),燃烧1mol C(石墨)放热393.51kJ.
C(金刚石)+O2(g)═CO2(g),燃烧1mol C(金刚石)放热395.41kJ.
可以得出的结论是( )
| A. | 金刚石比石墨稳定 | |
| B. | 1 mol石墨所具有的能量比1 mol金刚石低 | |
| C. | 金刚石转变成石墨是物理变化 | |
| D. | 石墨和金刚石都是碳的同位素 |
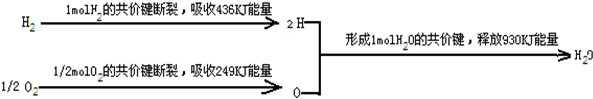
| A. | 1mol H2O 分解为H2与O2需吸收930 kJ热量 | |
| B. | H与O反应生成1mol H2O放出930 kJ热量 | |
| C. | 2 mol H的能量小于1mol H2的能量 | |
| D. | H结合成H2放出436 kJ的热量 |