题目内容
某混合气体X,可能由H2、CO、CO2和水蒸气中的一种或几种组成,现将混合气体通入灼热的CuO,完全反应后,固体CuO质量减少1.6 g;再将反应后的混合气体全部导入足量的澄清石灰水中,生成白色沉淀10 g。根据以上信息,分析下列有关X的组成推断正确的是( )
A.X一定只由CO组成
B.X一定只由H2和CO2组成
C.X可能由0.1 g H2和4.4 g CO2组成
D.X可能由0.1 g H2、1.4 g CO、2.2 g CO2组成
解析:选D 由反应后混合气体全部导入足量澄清石灰水中生成白色沉淀10 g可知,原混 合气体中碳元素的物质的量n(C)=n(CaCO3)=10 g÷100 g·mol-1=0.1 mol,即混合气体中存在CO、CO2中的一种或两种,且这两种含碳混合气体的物质的量或一种含碳气体的物质的量为0.1 mol,由此判断A项和B项错;假设混合气体中含碳气体只有CO2,则一定含有氢气,由混合气体通入灼热的CuO后,CuO质量减少1.6 g可知,氢气的物质的量n(H2)=1.6 g÷16 g·mol-1=0.1 mol,即其质量为0.2 g,C项错;选项D中氢气和CO均能还原CuO,二者“夺取”的CuO中的O为0.1 g÷2 g·mol-1+1.4 g÷28 g·mol-1=0.1 mol,与CuO减少的1.6 g氧原子相符,同时n(C)=1.4 g÷28 g·mol-1+2.2 g÷44 g·mol-1=0.1 mol,D项正确。
合气体中碳元素的物质的量n(C)=n(CaCO3)=10 g÷100 g·mol-1=0.1 mol,即混合气体中存在CO、CO2中的一种或两种,且这两种含碳混合气体的物质的量或一种含碳气体的物质的量为0.1 mol,由此判断A项和B项错;假设混合气体中含碳气体只有CO2,则一定含有氢气,由混合气体通入灼热的CuO后,CuO质量减少1.6 g可知,氢气的物质的量n(H2)=1.6 g÷16 g·mol-1=0.1 mol,即其质量为0.2 g,C项错;选项D中氢气和CO均能还原CuO,二者“夺取”的CuO中的O为0.1 g÷2 g·mol-1+1.4 g÷28 g·mol-1=0.1 mol,与CuO减少的1.6 g氧原子相符,同时n(C)=1.4 g÷28 g·mol-1+2.2 g÷44 g·mol-1=0.1 mol,D项正确。

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有还原性 |
仅用下表提供的实验操作或玻璃仪器(非玻璃仪器任选)就能够达到相应实验目的的是( )
| 选项 | 实验操作或玻璃仪器 | 实验目的 |
| A | 酸式滴定管、碱式滴定管、烧杯、锥形瓶 | 用0.01 mol/L的稀盐酸标定未知NaOH溶液的浓度 |
| B | 分液漏斗、锥形瓶、干燥管、导管、集气瓶 | 用碱石灰和浓氨水制备少量NH3 |
| C | 将浓硫酸和碳混合加热,直接将生成的气体通入足量的石灰水中,石灰水变浑浊 | 检验气体产物中CO2的存在 |
| D | 向某溶液中加入BaCl2溶液,产生白色沉淀 | 检验SO |
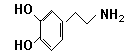 ⑴试判断多巴胺能发生的化学反应 。
⑴试判断多巴胺能发生的化学反应 。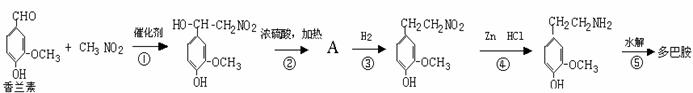 ⑶多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得。合成过程表示如下:
⑶多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得。合成过程表示如下:
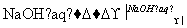 NaAlO2(aq)
NaAlO2(aq)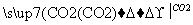 Al(OH)3
Al(OH)3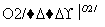 SO3
SO3 H2SO4
H2SO4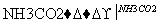 NaHCO3
NaHCO3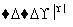 Na2CO3
Na2CO3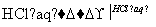 FeCl3(aq)
FeCl3(aq) 的存在
的存在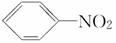 D.
D.
 B.
B.
 D.
D.