题目内容
【题目】二氯化二硫(S2C12)的结构式为Cl﹣S﹣S﹣Cl,易与水反应:2S2Cl2+2H2O=4HCl+SO2↑+3S↓.对该反应下列说法正确的是( )
A.S2C12做氧化剂,H2O做还原剂
B.氧化产物与还原产物的物质的量之比为l:3
C.每生成l mol SO2转移4 mol电子
D.每生成48g硫会断裂6mol共价键
【答案】B
【解析】解:A.只有S元素的化合价变化,则S2Cl2既作氧化剂又作还原剂,故A错误; B.氧化产物为SO2 , 还原产物为S,由反应可知二者的物质的量比为1:3,故B正确;
C.S元素的化合价由+1价升高为+4价,则每生成1molSO2转移3mol电子,故C错误;
D.48gS的物质的量为: ![]() =1.5mol,根据反应可知,生成1.5molS需要消耗1molCl﹣S﹣S﹣Cl和1molH2O,1molCl﹣S﹣S﹣Cl中含有3mol共价键,1mol水分子中含有2mol共价键,所以每生成48g硫会断裂5mol共价键,故D错误;
=1.5mol,根据反应可知,生成1.5molS需要消耗1molCl﹣S﹣S﹣Cl和1molH2O,1molCl﹣S﹣S﹣Cl中含有3mol共价键,1mol水分子中含有2mol共价键,所以每生成48g硫会断裂5mol共价键,故D错误;
故选B.
反应2S2Cl2+2H2O=4HCl+SO2↑+3S↓中,S元素的化合价由+1价升高为+4价,S元素的化合价由+1价降低为0,以此对各选项进行判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】下列实验方案中,能达到相应实验目的是( )
A | B | C | D | |
方案 |
|
|
|
|
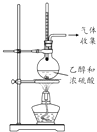
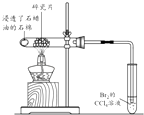
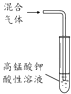
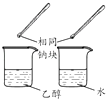
目的 | 利用乙醇的消去反应制取乙烯 | 验证石蜡油分解的产物是乙烯 | 检验乙烯、乙炔混合气中的乙烯 | 比较乙醇中羟基氢原子和水分子中氢原子的活泼性 |
A.A
B.B
C.C
D.D