题目内容
8.以电石、氯化钠、水为原料合成聚氯乙烯.某工厂日产聚氯乙烯塑料3.0t,若每步反应中原料的利用率都以95%计,试计算该工厂的月最大合理进料量(每月按30天计算).分析 逆推可知如下关系: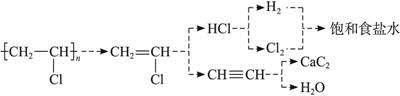
故题设条件下发生反应的化学方程式为:
①2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑
②H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl
③CaC2+2H2O→Ca(OH)2+C2H2↑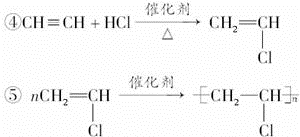
由上得关系式:n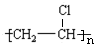 ~n CH2=CHCl~2n NaCl~n CaC2,据此计算.
~n CH2=CHCl~2n NaCl~n CaC2,据此计算.
解答 解:逆推可知如下关系:
故题设条件下发生反应的化学方程式为:
①2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑
②H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl
③CaC2+2H2O→Ca(OH)2+C2H2↑
由上得关系式:n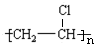 ~n CH2=CHCl~2n NaCl~n CaC2,则:
~n CH2=CHCl~2n NaCl~n CaC2,则:
n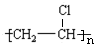 ~n CH2=CHCl~2n NaCl~n CaC2,
~n CH2=CHCl~2n NaCl~n CaC2,
62.5n 117n 64n
3.0t×30 m(NaCl)×0.95 m(CaC2)×0.95
m(NaCl)=$\frac{3.0t×30×117n}{62.5n×0.95}$=177.3t
m(CaC2)=$\frac{64n×3.0t×30}{62.5n×0.95}$=97.0t,
答:该工厂的月最大合理进料量:NaCl为177.3t,CaC2为97.0t.
点评 本题考查化学方程式有关计算,注意利用关系式解答,侧重考查学生分析计算能力,难度中等.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
5.对如图有机物的命名正确的是( )


| A. | 2一乙基一3,3一二,甲基戊烷 | B. | 3,3--甲基-4乙基戊烷 | ||
| C. | 3,3,4一三甲基己烷 | D. | 2,3,3一三甲基己烷 |
16.用NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A. | 82gNa218O2固体与足量的CO2反应转移电子数为NA | |
| B. | 0.1mol Mg在空气中完全燃烧生成氧化镁和二氮化三镁,转移电子数为0.2NA | |
| C. | 标准状况下,11.2L乙醇完全燃烧产生的CO2分子数NA | |
| D. | 1molCnH2n+2中含有的共价键数为(3n+1)NA |
3.下列物质中,含有离子键的是( )
| A. | H2O | B. | HCl | C. | CH4 | D. | NaOH |
20.取少量某有机物分别进行如下实验,结果是①能使酸性高锰酸钾溶液褪色;②与水混合静置后分层;③加入滴有酚酞试液的强碱,共热后酚酞变无色.此有机物是( )
| A. | 乙酸钠 | B. | 油酸甘油酯 | C. | 乙酸乙酯 | D. | 甲苯 |
17.4月22日是世界地球日,我国今年的地球日主题为:珍惜地球资源,转变发展方式,提高资源利用效益.下列有关做法与此不相符的是( )
| A. | 建立废旧电池回收站,对其进行回收再利用 | |
| B. | 将木材边角料制成木屑颗粒,用作环保能源 | |
| C. | 露天焚烧农作物秸秆还田,用作农作物肥料 | |
| D. | 部分煤炭转直接开采为先在地下气化或液化 |
18.在800℃下测定反应2NO+2H2═N2+2H2O的反应物初始浓度及反应的初速率,所得数据如表所示
下列分析实验数据所得的结论中不正确的是( )
| 实验标号 | 初始浓度/mol•L-1 | 生成N2的初速率/mol•L-1•s-1 | |
| c(NO) | c(H2) | ||
| 1 | 6.00×10-3 | 1.00×10-3 | 3.19×10-3 |
| 2 | 6.00×10-3 | 2.00×10-3 | 6.38×10-3 |
| 3 | 6.00×10-3 | 3.00×10-3 | 9.57×10-3 |
| 4 | 1.00×10-3 | 6.00×10-3 | 0.48×10-3 |
| 5 | 2.00×10-3 | 6.00×10-3 | 1.92×10-3 |
| 6 | 3.00×10-3 | 6.00×10-3 | 4.32×10-3 |
| A. | 增大c(H2),生成N2的初速率增大 | B. | 减小c(NO),生成N2的初速率减小 | ||
| C. | 生成N2的初速率与c(H2)成正比 | D. | 生成N2的初速率与c(NO)成正比 |
 某研究性小组为了探究石蜡油(17个碳以上的液态烷烃混合物)分解产物中有乙烯存在,设计了如下实验方案:
某研究性小组为了探究石蜡油(17个碳以上的液态烷烃混合物)分解产物中有乙烯存在,设计了如下实验方案: 已知A、B、C、D、E都是元素周期表中前36号元素,它们的原子序数依次增大.A原子基态时最外层电子数是其内层电子总数的2倍,B原子基态时s电子数与p电子数相等,C在元素周期表的各元素中电负性最大,D原子基态时最外层成对电子对数是单电子数的3倍,E原子基态时未成对电子数是同周期元素中最多的.
已知A、B、C、D、E都是元素周期表中前36号元素,它们的原子序数依次增大.A原子基态时最外层电子数是其内层电子总数的2倍,B原子基态时s电子数与p电子数相等,C在元素周期表的各元素中电负性最大,D原子基态时最外层成对电子对数是单电子数的3倍,E原子基态时未成对电子数是同周期元素中最多的. ,1mol A22-中含有的π键数目为2NA
,1mol A22-中含有的π键数目为2NA