题目内容
【题目】已知25 ℃、101 kPa时,1 mol H2与溴蒸气完全反应生成气态溴化氢放出能量Q kJ,则下列热化学方程式书写正确的是 ( )。
A.H2(g)+Br2(g)=2HBr(g) ΔH=-2Q kJ·mol-1
B.H2(g)+Br2(l)=2HBr(g) ΔH=-Q kJ·mol-1
C.![]() H2(g)+
H2(g)+![]() Br2(g)=HBr(g)ΔH=+
Br2(g)=HBr(g)ΔH=+![]() kJ·mol-1
kJ·mol-1
D.HBr(g)=![]() H2(g)+
H2(g)+![]() Br2(g)ΔH=+
Br2(g)ΔH=+![]() kJ·mol-1
kJ·mol-1
【答案】D
【解析】
已知25 ℃、101 kPa时,1 mol H2与溴蒸气完全反应生成气态溴化氢放出能量Q kJ,则热化学方程式为H2(g)+Br2(g)=2HBr(g) ΔH=-Q kJ·mol-1或![]() H2(g)+
H2(g)+![]() Br2(g)=HBr(g)ΔH=-
Br2(g)=HBr(g)ΔH=-![]() kJ·mol-,因此溴化氢分解的热化学方程式为HBr(g)=
kJ·mol-,因此溴化氢分解的热化学方程式为HBr(g)=![]() H2(g)+
H2(g)+![]() Br2(g)ΔH=+
Br2(g)ΔH=+![]() kJ·mol-1。答案选D。
kJ·mol-1。答案选D。

【题目】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸进行中和热的测定。
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体_____g。
(2)从下表中选择,称量NaOH固体所需要的仪器是(填字母)________。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如图所示。
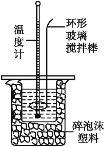
(1)若生成1 mol H2O时反应放出的热量为57.3 kJ,写出该反应的热化学方程式:__________。
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ______ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②用上述实验数值计算结果为____kJmol-1,与57.3 kJmol-1有偏差,产生偏差的原因可能是_____(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度