题目内容
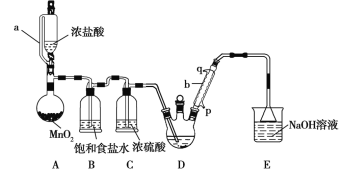
【题目】固体化合物X由3种元素组成。某学习小组进行了如下实验:
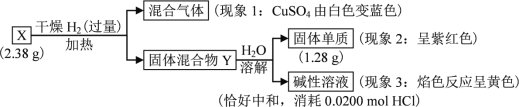
请回答:
(1) 由现象1得出化合物X含有________元素(填元素符号)。
(2) 固体混合物Y的成分________(填化学式)。
(3) X的化学式________。X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到蓝色溶液,该反应的化学方程式是________。
【答案】O Cu和NaOH NaCuO2 2NaCuO2+8HCl2NaCl+2CuCl2+Cl2↑+4H2O
【解析】
固体混合物Y溶于水,得到固体单质为紫红色,说明是Cu,产生碱性溶液,焰色反应呈黄色说明含有钠元素,与盐酸HCl中和,说明为NaOH(易算出为0.02mol),混合气体能使CuSO4变蓝,说明有水蒸汽。
(1)CuSO4由白色变为蓝色,说明有水生成,根据元素守恒分析,必定含有O元素。
(2)现象2获得紫色单质,说明Y含有Cu,现象3焰色反应为黄色说明有Na元素,与HCl发生中和反应说明有NaOH,故答案填Cu和NaOH。
(3)NaOH为0.02mol,易算出m(Na)=0.02×23g=0.46g,m(O)=m-m(Na)-m(Cu)=2.38-0.46-1.28=0.46g,N(Na):N(Cu):N(O)=![]() =1:1:2,故化学式为NaCuO2,X与浓盐酸反应,根据反应现象,产物有Cl2,和CuCl2蓝色溶液,因而化学方程式为2NaCuO2+8HCl2NaCl+2CuCl2+Cl2↑+4H2O
=1:1:2,故化学式为NaCuO2,X与浓盐酸反应,根据反应现象,产物有Cl2,和CuCl2蓝色溶液,因而化学方程式为2NaCuO2+8HCl2NaCl+2CuCl2+Cl2↑+4H2O

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案【题目】醋酸镍 ![]() 是一种重要的化工原料,一种以含镍废料
是一种重要的化工原料,一种以含镍废料![]() 含NiS、
含NiS、![]() 、FeO、CaO、
、FeO、CaO、![]() 为原料制取醋酸镍的工艺流程图如下图所示:
为原料制取醋酸镍的工艺流程图如下图所示:
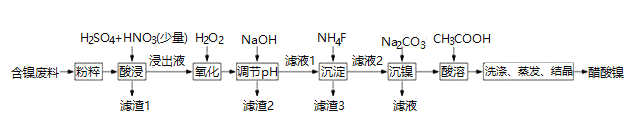
相关离子生成氢氧化物的pH和相关物质的溶解性如表:
金属离子 | 开始沉淀时的pH | 沉淀完全时的pH | 物质 |
|
|
|
|
| 微溶 |
|
|
|
| 可溶 |
|
|
|
| 难溶 |
|
|
|
|
|
![]() 的电子式为_________________。
的电子式为_________________。
![]() 调节pH步骤中,溶液pH的调节范围是_________________。
调节pH步骤中,溶液pH的调节范围是_________________。
![]() 滤渣1和滤渣3主要成分的化学式分别是_________________、_________________。
滤渣1和滤渣3主要成分的化学式分别是_________________、_________________。
![]() 酸浸过程中,lmolNiS失去
酸浸过程中,lmolNiS失去![]() 个电子,同时生成两种无色有毒气体,写出该反应的化学方程式:________。
个电子,同时生成两种无色有毒气体,写出该反应的化学方程式:________。
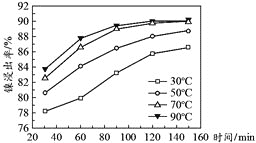
![]() 保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如下图所示,酸浸的最佳温度与时间分别为_________________。
保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如下图所示,酸浸的最佳温度与时间分别为_________________。
![]() 沉镍过程中,若
沉镍过程中,若![]() ,欲使100mL该滤液中的
,欲使100mL该滤液中的![]() 沉淀完全
沉淀完全![]() ,则需要加入
,则需要加入![]() 固体的质量最少为___________
固体的质量最少为___________![]() 保留小数点后2位有效数字
保留小数点后2位有效数字![]() 。
。
![]() 近年来镍氢电池发展很快,它可由
近年来镍氢电池发展很快,它可由![]() 跟
跟![]() 中各元素化合价均可看作是零
中各元素化合价均可看作是零![]() 组成:
组成:![]()
![]()
![]() 。该电池放电时,负极反应是________。
。该电池放电时,负极反应是________。