题目内容
盛有NO和NO2的混合气体的量筒倒立在盛有水的水槽中,过一段时间后,量筒内的气体体积减小为原来的一半.则原混合气体中NO和NO2的体积比是( )
分析:NO2通入水中,发生:3NO2+H2O=2HNO3+NO,根据反应的化学方程式计算.
解答:解:NO2通入水中,发生:3NO2+H2O=2HNO3+NO,
设混合气体中含有xmolNO,ymolNO2,过一段时间后,量筒内的气体体积减小为原来的一半,则物质的量减小一半,
3NO2+H2O=2HNO3+NO
3 1
ymol
mol
则:
=
,
解之得:x:y=1:3,
故选B.
设混合气体中含有xmolNO,ymolNO2,过一段时间后,量筒内的气体体积减小为原来的一半,则物质的量减小一半,
3NO2+H2O=2HNO3+NO
3 1
ymol
| y |
| 3 |
则:
x+
| ||
| x+y |
| 1 |
| 2 |
解之得:x:y=1:3,
故选B.
点评:本题考查混合物的计算,题目难度不大,本题注意混合气体通入水中,体积减小的原因是二氧化氮与水反应的缘故,根据反应的化学方程式计算.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能( )| A、是NO2一种气体 | B、是NH3与NO2的混和气体 | C、是NO与NO2的混和气体 | D、是CO与NO2的混和气体 |
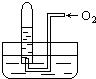 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能是( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能是( )| A、可能是N2与NO2的混和气体 | B、可能是O2与NO2的混和气体 | C、可能是NO与NO2的混和气体 | D、可能是NO2一种气体 |
 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( ) 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能是( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能是( ) 铁是人类生产和生活中必不可少的重要金属(如图).
铁是人类生产和生活中必不可少的重要金属(如图).